
【题目】水溶液中的离子平衡是中学学习的一个重要内容。
(1)甲同学用pH试纸分别测定了 0.1 mol/L NaOH溶液的pH=13、0.1 mol/LCH3COOH溶液的pH=3、0.001 mol/L HCl溶液的pH=3。请写出pH试纸使用方法:_____根据测量结果,甲推测等浓度的NaOH溶液、CH3COOH溶液中,由水电离出的H+浓度c(H+)NaOH____c(H+)CH3COOH(填“大于”“小于”或“等于”)
(2)乙同学分别取了pH=3的CH3COOH溶液和HCl溶液各10mL,测量导电能力发现HCl溶液导电能力______________CH3COOH溶液导电能力(填“大于”“小于”或“等于”)。然后分别加水稀释到100 mL后,再次测量,稀释后的HCl溶液导电能力______________CH3COOH溶液导电能力(填“大于”“小于”或“等于”)
(3)丙同学查阅资料发现,人体血液里存在重要的酸碱平衡:CO2+H2O![]() H2CO3
H2CO3![]() HCO3-,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
HCO3-,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
c(HCO3-) ∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
①正常人体血液中,HCO3-的水解程度____电离程度(填“>”、“<”或“=”);
②人体血液酸中毒时,可注射________(填选项)缓解;
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小顺序___________
④已知25 ℃时,CO32-水解反应的平衡常数Kh=![]() =
= =2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,溶液的pH=________;
=2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,溶液的pH=________;
(4)丁同学探究难溶电解质在水溶液中的性质,查阅资料发现25 ℃时,AgCl的Ksp=1.8×10-10,该温度下向1 L 0.03 mol/L的AgNO3溶液中加入1 L 0.01 mol/L的NaCl溶液之后,溶液中c(Cl-)=______mol/L(忽略混合前后溶液体积的变化)。平衡后,若向该体系中再加入少量AgCl固体,则c(Cl-)_____(填“增大”或“减小”或“span>不变”)。
【答案】把一小块pH试纸放在表面皿(或玻璃片)上,用玻璃棒蘸取少量待测液点在试纸的中部,变色后与标准比色卡对照读数 小于 等于 小于 > B c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) pH=10 1.8×10-8 不变
【解析】
(1)用pH试纸测定溶液的pH不能湿润;根据溶液中离子浓度对水电离平衡移动的影响分析比较溶液中水电离产生的离子浓度大小;
(2)溶液的导电性与溶液中微粒的浓度及离子带有的电荷数目有关,与微粒的种类无关;
醋酸是弱酸,在溶液中存在电离平衡,根据稀释对溶液中离子浓度的影响分析判断溶液的导电性;
(3)①根据人体血液的酸碱性确定碳酸氢根离子的电离和水解程度相对大小;
②发生酸中毒时,应该用碱性物质缓解;
③等浓度的Na2CO3和NaHCO3的混合,溶液由于水解而显碱性,根据物料守恒和两种盐的水解程度大小分析比较溶液中各离子浓度大小;
④已知25 ℃时,CO32-水解反应的平衡常数Kh=![]() =
= =2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,将数值带入,同时结合水的离子积常数及pH=-lgc(H+)溶液的pH;
=2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,将数值带入,同时结合水的离子积常数及pH=-lgc(H+)溶液的pH;
(4)先根据AgNO3、NaCl溶液中溶质的物质的量,结合二者反应关系判断哪种物质过量,计算出过量离子的物质的量浓度,利用Ksp(AgCl)计算出c(Cl-),在溶液中存在沉淀溶解平衡,根据固体与溶解平衡关系分析判断离子浓度情况。
(1)pH试纸的使用方法是:把一小块pH试纸放在表面皿(或玻璃片)上,用玻璃棒蘸取少量待测液点在试纸的中部,待变色后与标准比色卡对照读数;
0.1 mol/L NaOH溶液的pH=13,则c(OH-)=0.1mol/L;0.1 mol/LCH3COOH溶液的pH=3,则c(H+)=10-3mol/L,说明NaOH是一元强碱,醋酸是一元弱酸,等浓度的NaOH、CH3COOH溶液中离子浓度NaOH的大于醋酸的,由于在两种物质的溶液中都存在H2O的电离平衡:H2O![]() H++OH-,等浓度的H+、OH-对水的电离平衡抑制作用相同,由于等浓度的NaOH溶液中的离子浓度大于醋酸溶液中的离子浓度,所以对水的抑制作用NaOH>CH3COOH,故由水电离出的H+浓度c(H+)NaOH<c(H+)CH3COOH;
H++OH-,等浓度的H+、OH-对水的电离平衡抑制作用相同,由于等浓度的NaOH溶液中的离子浓度大于醋酸溶液中的离子浓度,所以对水的抑制作用NaOH>CH3COOH,故由水电离出的H+浓度c(H+)NaOH<c(H+)CH3COOH;
(2)溶液的导电性与溶液中微粒的浓度及离子带有的电荷数目有关,与微粒的种类无关。pH=3的CH3COOH溶液和HCl溶液各10mL,离子的浓度相等,离子所带电荷相同,所以溶液的导电能力也相等;
醋酸是一元弱酸,在溶液中存在电离平衡,c(CH3COOH)>c(H+),将两者10mL分别加水稀释到100 mL后,由于HCl是一元强酸,完全电离,稀释使溶液中离子浓度降低,而在CH3COOH溶液在存在电离平衡,稀释电离平衡正向移动,又使溶液中的离子浓度增大,最终达到平衡时,溶液中离子浓度CH3COOH溶液>HCl溶液,故稀释相同倍数后溶液的导电性:HCl<CH3COOH;
(3)①人体血液pH值保持在7.35~7.45之间,说明HCO3-的水解程度大于电离程度;
②发生酸中毒时,应用碱性物质缓解;
A.NaOH溶液是强碱溶液,具有强腐蚀性,不能使用,A不符合题意;
B.NaHCO3溶液水解显碱性,可以和酸反应起到缓解人体血液酸中毒,B符合题意;
C.NaCl溶液是中性溶液不起作用,C不符合题意;
D.Na2SO4溶液是中性溶液不能缓解血液的酸性,D不符合题意;
故合理选项是B;
③等浓度的Na2CO3和NaHCO3的混合,根据电解质的电离可知c(Na+)最大,由于Na2CO3和NaHCO3水解使溶液显碱性,所以c(OH-)>c(H+),水解程度CO32->HCO3-,则c(HCO3-)>c(CO32-),盐电离产生的离子浓度远大于水电离产生的H+、OH-的浓度,所以c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故该混合溶液中各离子浓度大小顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
④已知25 ℃时,CO32-水解反应的平衡常数Kh=![]() =
= =2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,Kh=
=2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,Kh= =2×c(OH-)=2×10-4 mol/L,所以c(OH-)=1×10-4 mol/L,c(H+)=10-10mol/L所以溶液的pH=10;
=2×c(OH-)=2×10-4 mol/L,所以c(OH-)=1×10-4 mol/L,c(H+)=10-10mol/L所以溶液的pH=10;
(4)1 L 0.03 mol/L的AgNO3溶液中加入1 L 0.01mol/L的NaCl溶液后,二者发生反应:Ag++Cl-=AgCl↓,根据反应关系可知:硝酸银过量,氯化钠完全反应,剩余的硝酸银浓度c(AgNO3)=c(Ag+)=![]() =0.01mol/L,根据AgCl的Ksp=1.8×10-10,可知c(Cl-)=
=0.01mol/L,根据AgCl的Ksp=1.8×10-10,可知c(Cl-)=![]() =1.8×10-8;反应后AgCl溶液形成沉淀溶解平衡体系,加入氯化银固体不影响平衡,因此溶液中氯离子浓度不变。
=1.8×10-8;反应后AgCl溶液形成沉淀溶解平衡体系,加入氯化银固体不影响平衡,因此溶液中氯离子浓度不变。


科目:高中化学 来源: 题型:
【题目】工业上在一定条件下将丙烷脱氢制丙烯.
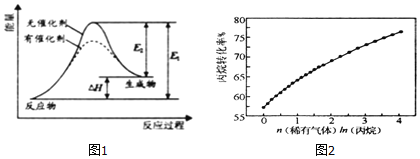
![]() 反应过程中能量变化如图1所示,下列有关叙述正确的是______.
反应过程中能量变化如图1所示,下列有关叙述正确的是______.
![]() 此反应为吸热反应
此反应为吸热反应
![]() 催化剂能改变反应的焓变和活化能
催化剂能改变反应的焓变和活化能
![]() 表示正反应的活化能,
表示正反应的活化能,![]() 表示逆反应的活化能
表示逆反应的活化能
![]() 有催化剂能加快反应速率,提高丙烷的转化率
有催化剂能加快反应速率,提高丙烷的转化率
![]() 上述反应在恒温恒容密闭容器中达到平衡,其平衡常数K的表达式为______
上述反应在恒温恒容密闭容器中达到平衡,其平衡常数K的表达式为______![]() 若升温,该反应的平衡常数______
若升温,该反应的平衡常数______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() 若向上述反应达到平衡的容器内再通入少量丙烷,则
若向上述反应达到平衡的容器内再通入少量丙烷,则![]() ______
______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() .
.
![]() 在
在![]() 、800K条件下,向恒容密闭容器中通入丙烷和稀有气体,丙烷脱氢反应的转化率随着稀有气体与丙烷比例的变化情况如图2所示,则随着稀有气体与丙烷比例的增加,丙烷转化率逐渐增大的原因是______.
、800K条件下,向恒容密闭容器中通入丙烷和稀有气体,丙烷脱氢反应的转化率随着稀有气体与丙烷比例的变化情况如图2所示,则随着稀有气体与丙烷比例的增加,丙烷转化率逐渐增大的原因是______.
![]() 上述反应生成物丙烯经多步氧化生成丙酸,已知常温下
上述反应生成物丙烯经多步氧化生成丙酸,已知常温下![]() .
.
![]() 用离子方程式表示
用离子方程式表示![]() 溶液显碱性的原因______.
溶液显碱性的原因______.
![]() 常温下,若丙酸与氨水混合后溶液呈中性,则溶液中
常温下,若丙酸与氨水混合后溶液呈中性,则溶液中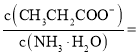 ______.
______.
![]() 已知:
已知:
化学键 |
|
|
|
|
键能 | 436 | 413 | 348 | 612 |
则丙烷脱氢反应的热化学方程式为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中加入4 mol A和2 mol B进行反应:3A(g)+2B(g) ![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后的压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后的压强之比为5∶4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=
B.此时,B的平衡转化率是35%
C.增大该体系的压强,平衡正向移动,化学平衡常数增大
D.增加C,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用50mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
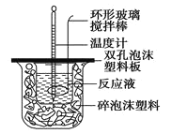
(1)烧杯间填满碎泡沫塑料的作用是______________;
(2)环形玻璃搅拌棒_______(填“能”或“不能”)用环形铁质搅拌棒代替,其原因是________;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是___________。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量______ (填“相等”“不相等”),若实验操作均正确,则所求中和热_______ (填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:________。
Ⅱ.FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。已知25℃,101 kPa时:
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1648 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480 kJ·mol-1
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
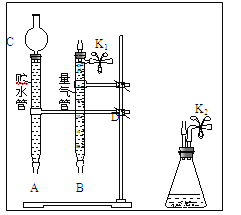
(1)现有以下仪器和用品:橡胶管、秒表、温度计、amol/L稀硝酸、bmol/L稀硝酸及下图中仪器.
①写出本实验的化学方程式,并标出电子转方向和数目:__________________________.
②设计实验方案:在_________________下,测定________________________________.
③在答卷的图中将A、B、C、D、几处用橡胶管以正确方式连接起来,以测定反应所产生气体的体积(三个容器中的液体和水都已画出)_______________.
④测定前,为避免NO被氧化为NO2,要用CO2排出锥形瓶和橡胶管中的空气:在锥形瓶中加入铜片后松开K2弹簧夹,从K2处的橡胶管向装置中通入CO2,此时K1处应进行的操作是____________,则空气已排尽.
(2)注入稀硝酸后,在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间t1、t2、t3;收集气体体积V1、V2.请完成下表:____________
实验 | 稀硝酸的浓度/(mol/L) | 稀硝酸的体积/mL | 温度 | 时间 | 收集气体 |
① | a | V | 25 | t1 | V1 |
② | V | ||||
③ | V |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应2XY(g)![]() X2(g)+Y2(g) 达到平衡的标志是
X2(g)+Y2(g) 达到平衡的标志是
A. 单位时间内,生成nmolX2的同时,生成nmolXY
B. 单位时间内, 生成nmolX2的同时,生成nmolY2
C. 单位时间内,生成2nmolXY的同时,消耗nmolY2
D. 单位时间内,生成nmolX2的同时,消耗nmolY2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验某溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作.其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是![]()
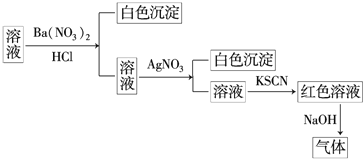
A.原溶液中一定含有![]() B.原溶液中一定含有
B.原溶液中一定含有![]()
C.原溶液中一定含有![]() D.原溶液中一定含有
D.原溶液中一定含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中含有右表离子中的某5种,且其浓度均为![]() 不考虑水的电离与离子水解
不考虑水的电离与离子水解![]() 向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
阳离子 | 阴离子 |
Fe Fe |
|
A.X溶液中不可能含有![]() 或
或![]()
B.生成无色气体的离子方程式为:![]()
C.根据电荷守恒,原溶液中一定含![]()
D.X溶液中一定含3种阳离子、2种阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A.标准状况下,22.4 L CH2Cl2中含有碳原子数为NA
B.在溶有1molFe(OH)3的胶体中含有的胶粒数小于NA
C.常温下0.2 mol铝与足量浓硫酸反应,生成气体的分子数为0.3 NA
D.常温下向密闭容器内充入46 g NO2,容器中气体的分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com