
用标准盐酸滴定一种由![]() 组成的混合溶液,以便确定各组分的含量。已知
组成的混合溶液,以便确定各组分的含量。已知![]() 时,
时,![]() 全部转变为
全部转变为![]() ,则滴定中选择的指示剂应为
,则滴定中选择的指示剂应为
A. 先用酚酞后用甲基橙 B. 先用酚酞后用石蕊
C. 先用石蕊后用甲基橙 D. 先用甲基橙后用酚酞
科目:高中化学 来源: 题型:阅读理解
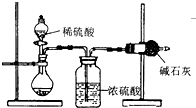 测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:
测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:| 106n |
| 197m |
| 106n |
| 197m |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
双指示剂法可用来测定试样中含有NaOH、NaHCO3和Na2CO3中的一种或两种物质的含量。具体做法:先向待测溶液中加入酚酞,用标准盐酸滴定,当NaOH或Na2CO3转化为NaCl或NaHCO3时,溶液褪为无色,消耗V1mL盐酸。然后滴加甲基橙,继续用标准盐酸滴定,当NaHCO3转化为NaCl时,溶液由黄色变为橙色,消耗V2mL盐酸。
(1)试根据下表给出的V1、V2的数据范围判断原混合物的成分(用化学式表示)。
(2)若称取含杂质的试样1.200g(杂质不与HCl反应)配制成100.0mL水溶液,取出20.00mL,用0.1000mol/L标准盐酸滴定,测得V1=35.00mL,V2=5.00mL。求试样的成分及各成分的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
双指示剂法可用来测定NaOH、NaHCO3、Na2CO3中的一种或两种物质组成的混合物的含量。做法是:先向待测液中加酚酞,用标准盐酸滴定,当NaOH或Na2CO3被转化为NaCl或NaHCO3时,酚酞由红色褪为无色,消耗V1 mL盐酸,然后滴加甲基橙,继续用盐酸滴定,当NaHCO3转化为NaCl时,溶液由黄色变为橙色,消耗V2 mL盐酸。
思考:(1)今用上法进行下表5种试样测试,试根据盐酸用量确定①~⑤的成分。
试样 | ① | ② | ③ | ④ | ⑤ |
标准盐酸用量 | V1>V2 且V2=0 | V1<V2 且V1=0 | V1=V2 且V2>0 | V1>V2>0 | V2>V1>0 |
试样成分 |
|
|
|
|
|
(2)若称取含杂质试样1.2 g(杂质不与盐酸反应),配制成100 mL水溶液,取出20 mL,用0.1 mol·L-1盐酸滴定,测得V1=35 mL,V2=5 mL,求试样的成分及其质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com