
A、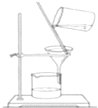 过滤 |
B、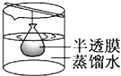 渗析 |
C、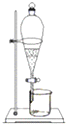 萃取 |
D、 丁达尔效应 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
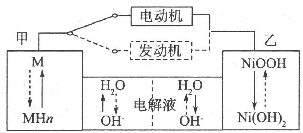 第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.其电路工作原 理如图所示.下列说法中正确的是( )
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆.汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态.其电路工作原 理如图所示.下列说法中正确的是( )| A、电池充电时,OH-由甲侧向乙侧移动 |
| B、甲放电时为正极,充电时为阳极 |
| C、放电时正极的电极反应式为MHn-ne-═M+nH+ |
| D、汽车下坡时发生图中实线所示的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
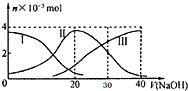 25℃时,向20mL 0.2mol/L H2A(某二元弱酸)溶液中滴加0.2mol/L NaOH溶液,有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)?根据图示判断,下列说法中正确的是( )
25℃时,向20mL 0.2mol/L H2A(某二元弱酸)溶液中滴加0.2mol/L NaOH溶液,有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)?根据图示判断,下列说法中正确的是( )| A、当V(NaOH)=20mL时,所得溶液中:c(OH-)>c(H+) |
| B、当V(NaOH)=30mL时,所得溶液中:2c(H+)+c(HA-)+3c(H2A)=c(A2-)+2 c(OH-) |
| C、当V(NaOH)=40mL时,所得溶液中:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) |
| D、在NaHA溶液中:c(OH-)+2c(A2-)=c(H+)+2c(H2A) |
查看答案和解析>>
科目:高中化学 来源: 题型:
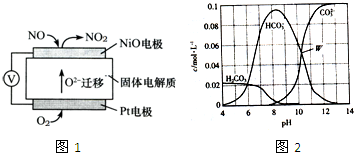 根据化学反应原理,回答下列问题:
根据化学反应原理,回答下列问题:c(HC
| ||
c(C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2=Ca2++2OH- |
| B、NaOH=Na++O2-+H+ |
| C、HCl=H++Cl- |
| D、K2SO4=2K++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅是一种亲氧元素,在自然界中它总是与氧相互化合的 |
| B、氯气是一种有毒的黄绿色气体,但可用于自来水的杀菌消毒 |
| C、为了防止食品受潮及富脂食品氧化变质,常在包装袋中放入硅胶和硫酸亚铁 |
| D、白色污染、绿色食品中的“白”、“绿”均指相关物质的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com