
【题目】关于下列各图的叙述错误的是![]()
化学方程式 | 平衡常数K |
|
|
|
|
|
|
|
|
A.已知1molCO燃烧放出的热为283kJ,![]() ;
;![]() 则
则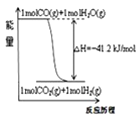 表示CO和
表示CO和![]() 生成
生成![]() 和
和![]() 的能量变化
的能量变化
B.常温下![]()
![]() HB溶液和
HB溶液和![]()
![]() 溶液等体积混合后溶液的
溶液等体积混合后溶液的![]() ,则混合溶液中离子浓度的大小顺序为:
,则混合溶液中离子浓度的大小顺序为:![]()
C.常温下,![]() 和
和![]() 反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时
反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时![]() 从
从![]() 到
到![]() 的转化率逐减小,且HX的还原性逐渐减弱
的转化率逐减小,且HX的还原性逐渐减弱
D.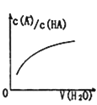 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,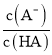 的变化情况
的变化情况
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mol/L某一元酸HA 在水中电离度为0.02%,回答下列各问题:
(1)该溶液中c(H+)=_________。
(2)HA的电离平衡常数K=_________;
(3)升高温度时,K_________ (填“增大”,“减小”或“不变”)。
(4)由HA电离出的c(H+)约为水电离出的c(H+)的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)与葡萄糖相似具有强还原性,40%甲醛溶液沸点为96℃,易挥发。为探究过量甲醛和新制Cu(OH)2反应的产物,进行如下研究。
(1)在如图装置中进行实验,向a中加入0.5mol/LCuSO4溶液50mL和5mol/LNaOH溶液100mL,振荡,再加入40%的甲醛溶液40mL,缓慢加热a,在65℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红色,并有气体产生。
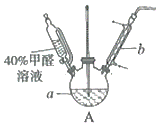
①仪器a的名称是__,仪器b的作用为__。
②能说明甲醛具有还原性的实验现象是__。
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物含H2不含CO,将装置A和如图所示的装置连接后进行实验。
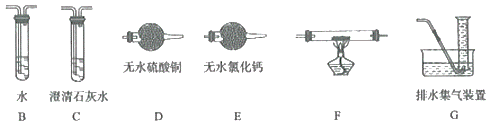
①依次连接的合理顺序为A→B→___→____→___→___→G;___
②装置B的作用是___;
③确认气体产物中含H2而不含CO的现象是___。
(3)已知:![]()
![]()
![]()
![]()
![]() 。设计实验证明a中甲醛的碳元素未被氧化成+4价的实验方案为:取少量a中反应后的清液,___,则说明甲醛的碳元素未被氧化成+4价。
。设计实验证明a中甲醛的碳元素未被氧化成+4价的实验方案为:取少量a中反应后的清液,___,则说明甲醛的碳元素未被氧化成+4价。
(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应):
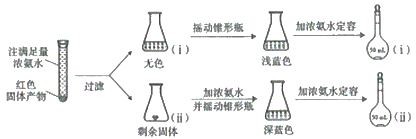
已知:i:Cu2O![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+(蓝色)。
[Cu(NH3)4]2+(蓝色)。
ⅱ:2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示。下列关于整个反应过程中的叙述错误的是
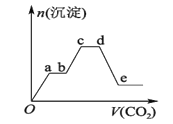
A. Oa段反应的化学方程式是Ba(OH)2+CO2 =BaCO3↓+H2O
B. bc段与cd段所消耗CO2的体积相同
C. bc段反应的离子方程式是2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32-
D. de段沉淀减少是由于BaCO3固体的消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢镍电池是近年开发出的可充电电池,电池的总反应式为1/2 H2 + NiO(OH) ![]() Ni(OH)2 ,下列叙述正确的是( )
Ni(OH)2 ,下列叙述正确的是( )
A.电池充电时,Ni元素被还原B.电池放电时,镍元素被氧化
C.电池充电时,只有H元素被氧化D.电池放电时,氢气中氢元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下HF的电离常数Ka=3.3×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
A. 该温度下,0.31 mol·L-1的HF溶液的pH=2
B. 升高温度或增大浓度,HF的电离平衡常数都将增大
C. 两溶液混合不会产生沉淀
D. 向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向![]() 溶液中逐滴加入NaOH溶液,所得溶液中
溶液中逐滴加入NaOH溶液,所得溶液中![]() ,
,![]() ,
,![]() 三者物质的量分数
三者物质的量分数![]() 分布系数
分布系数![]() 随PH变化的关系入图1所示。图2为不同浓度
随PH变化的关系入图1所示。图2为不同浓度![]() 溶液中部分微粒浓度。下列表述错误的是
溶液中部分微粒浓度。下列表述错误的是![]()
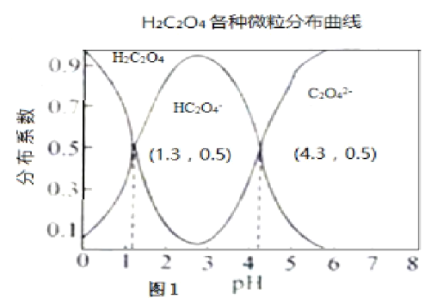
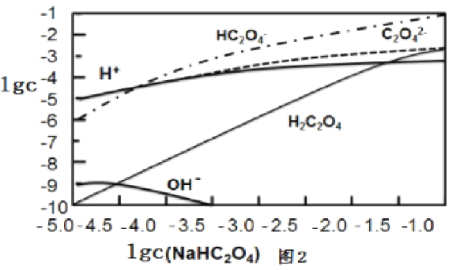
A.![]()
B.将等物质的量的![]() 、
、![]() 溶于水中,所得溶液PH恰好为
溶于水中,所得溶液PH恰好为![]()
C.![]() 溶液中一定存在
溶液中一定存在![]() ,同时
,同时![]()
D.在![]()
![]() 溶液中各离子浓度大小关系为:
溶液中各离子浓度大小关系为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式如图所示:下列有关说法正确的是( )
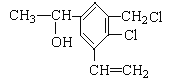
A.该有机物的化学式为C11H12OCl2
B.在同一平面上的碳原子数最多为10个
C.与NaOH醇溶液在加热条件下消去氯原子
D.在铜作催化剂和加热条件下能被O2氧化成醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③HCl气体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.②④⑥B.①②C.②③⑤D.②④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com