
| A. | 称氢氧化钠时,不能直接称量,也不能放在称量纸上 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从下口倒出 | |
| D. | 过滤时,玻璃棒的末端应轻轻靠在三层的滤纸上 |
分析 A.氢氧化钠有腐蚀性易潮解;
B.蒸馏时,测定馏分的温度;
C.分液时,避免上下层液体混合;
D.根据过滤实验操作的规范性判断.
解答 解:A.氢氧化钠有腐蚀性易潮解,不能直接称量,也不能放在称量纸上,应在小烧杯中称量,故A正确;
B.蒸馏时,测定馏分的温度,则使温度计的水银球放置于蒸馏烧瓶的支管口处,故B正确;
C.分液时,避免上下层液体混合,则分液漏斗中下层液体从下口放出,上层液体从上口倒出,故C错误;
D.过滤时,为防止玻璃棒弄坏滤纸,应将玻璃棒在引流过程中放在三层滤纸处,故D正确.
故选C.
点评 本题主要考查了蒸馏、分液、过滤、称量等实验基本操作,难度不大,称取药品时要注意:左物右码;分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出.


科目:高中化学 来源: 题型:解答题
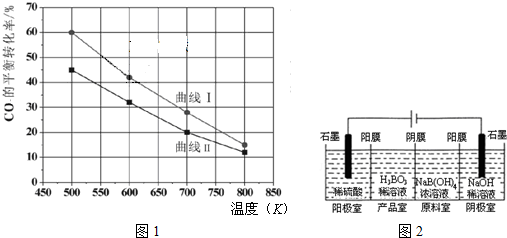
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/mn | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 | |
| B. | 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 | |
| C. | 元素②⑥形成的化合物具有两性 | |
| D. | 元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
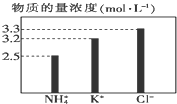
| A. | 2、64、24 | B. | 64、2、24 | C. | 64、24、2 | D. | 16、2、24 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 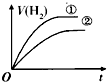 | C. | 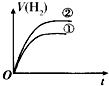 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硝酸保存在无色玻璃瓶中 | |
| B. | 金属钠和钾保存在煤油中 | |
| C. | Na2CO3可以保存在玻璃塞的玻璃瓶中 | |
| D. | NaOH固体放在滤纸上称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | T2 |
| 水的离子积常数 | 1×10-14 | 1×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com