
 B.
B. C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH
C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH分析 (1)根据乙醇的物理性质分析;
(2)乙烯中含双键可和水发生加成反应生成乙醇;
(3)根据同分异构体的概念分析;
(4)①计算出乙醇的物质的量,根据方程式分析;
②根据题给信息可知反应物和生成物,写出方程式配平即可.
解答 解:(1)乙醇的密度比水小,
故答案为:小;
(2)乙烯中含双键可和水发生加成反应生成乙醇,反应方程式为:CH2═CH2+H2O$→_{△}^{催化剂}$CH3CH2OH,从方程式可看出,反应物全部转化为生产物,原子利用率为100%,
故答案为:CH2═CH2+H2O$→_{△}^{催化剂}$CH3CH2OH;100%;
(3)分子式相同结构不同的有机物互称同分异构体,故乙醇的同分异构体为甲醚;
故答案为:D;
(4)①46g乙醇的物质的量为:$\frac{46g}{46g/mol}$=1mol,C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O,所用1mol乙醇燃烧消耗3mol氧气,
故答案为:3;
②乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查了乙醇的性质和结构,题目难度不大,注意乙醇的催化氧化为高频考点.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-Cl-O | B. | 14C的原子结构示意图: | ||
| C. | 聚氯乙烯的结构简式: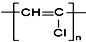 | D. | 丙烷分子的球棍模型示意图: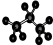 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧生成白色的氧化钠固体 | |
| B. | 检验FeCl2溶液中的少量Fe3+,可以用KSCN溶液 | |
| C. | 二氧化硫的水溶液能使紫色石蕊溶液变红,随后使之褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:c>b>a | |
| B. | a与c形成化合物的溶液有毒,要密封保存于玻璃瓶中 | |
| C. | a2b2与d的一种较高价态离子的盐溶液混合时会产生大量的b2 | |
| D. | d高价离子在溶液中与c的低价离子因发生氧化还原反应而不能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用填埋法处理未经分类的生活垃圾 | |
| B. | “地沟油”经过加工处理后可用来制肥皂 | |
| C. | 大量使用薪柴为燃料,践行低碳生活 | |
| D. | CO2、NO2或SO2的排放是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2[ | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com