
ЁОЬтФПЁПФГЮТЖШЪБЃЌТБЛЏвј(AgX, X=ClЃЌBr,I)ЕФ3ЬѕШмНтЦНКтЧњЯпШчЯТЭМЫљЪОЃЌAgClЁЂAgBrЁЂAgIЕФKspвРДЮМѕаЁ.вбжЊpAg=-lgc(Ag+)ЃЌpX=-lgc(X-),РћгУpXЁЂpAgЕФзјБъЯЕПЩБэЪОГіAgXЕФШмЖШЛ§гыШмвКжаЕФc(Ag+)КЭc(X-)ЕФЯрЛЅЙиЯЕЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ

A. AЯпЪЧAgClЕФШмНтЦНКтЧњЯп
B. зјБъЕуpаЮГЩЕФШмвКЪЧAgClЕФВЛБЅКЭШмвК
C. mЕуЪЧдкЫЎжаМгШызуСПЕФAgBrаЮГЩЕФБЅКЭШмвК
D. nЕуБэЪОгЩЙ§СПЕФKIгыAgNO3ЗДгІВњЩњAgIГСЕэ
ЁОД№АИЁПD
ЁОНтЮіЁПAЃЎвбжЊpAg=-lgcЃЈAg+ЃЉЃЌpX=-lgcЃЈX-ЃЉЃЌвјРызгЁЂТШРызгХЈЖШдНДѓЃЌХЈЖШЕФИКЖдЪ§ЕУЕНЪ§жЕдНаЁЃЌвРОнЭМЯѓЗжЮіПЩжЊЃЌШмНтЖШЃКТШЛЏвјЃОфхЛЏвјЃОЕтЛЏвјЃЌШмвКжаЕФРызгХЈЖШвВЪЧТШЛЏвјЃОфхЛЏвјЃОЕтЛЏвјЃЌЫљвдAЯпБэЪОЕФЪЧAgClЃЌBЯпБэЪОЕФЪЧAgBrЃЌCЯпБэЪОЕФЪЧAgIЃЌAе§ШЗЃЛBЃЎзјБъЕуpВЛдйЧњЯпЩЯЃЌаЮГЩЕФШмвКЪЧAgClЕФВЛБЅКЭШмвКЃЌBе§ШЗЃЛCЃЎmЕуЪЧГСЕэШмНтЦНКтЯпЩЯЕФвЛЕуЃЌЫЕУїЪЧГСЕэШмНтЦНКтзДЬЌЯТЕФБЅКЭШмвКЃЌCе§ШЗЃЛDЃЎвђЮЊnЕудкЧњЯпЩЯЃЌМДДІгкГСЕэ-ШмНтЦНКтзДЬЌЃЌВЛДцдкОЛЩњГЩГСЕэЛђгаВПЗжГСЕэШмНтЕФЮЪЬтЃЌБэЪОЕФЪЧЕтЛЏвјГСЕэЕФШмНтГСЕэЦНКтзДЬЌЃЌDДэЮѓЃЛД№АИбЁDЁЃ


 УћЪІАщФуГЩГЄПЮЪБЭЌВНбЇСЗВтЯЕСаД№АИ
УћЪІАщФуГЩГЄПЮЪБЭЌВНбЇСЗВтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПэкЪЧЂіAзхдЊЫиЃЌЦфЕЅжЪКЭЛЏКЯЮядкЛЏЙЄЩњВњЕШЗНУцОпгаЙуЗКгІгУЁЃ
ЃЈ1ЃЉTeO2ЪЧСНадбѕЛЏЮяЃЌЮЂШмгкЫЎЃЌПЩШмгкЧПЫсЁЂЛђЧПМюЁЃTeO2КЭNaOHШмвКЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______________ЁЃ
ЃЈ2ЃЉэкЫсЃЈH6TeO6ЃЉЪЧвЛжжКмШѕЕФЫсЃЌKa1=1ЁС10-7ЃЌИУЮТЖШЯТ0.1mol/L H6TeO6ЕФЕчРыЖШІСЮЊ_____ЃЈНсЙћБЃСєвЛЮЛгааЇЪ§зжЃЉЁЃдкЫсадНщжЪжаЃЌэкЫсПЩНЋHIбѕЛЏГЩI2ЃЌШєЗДгІЩњГЩЕФTeO2гыTeЕФЮяжЪЕФСПжЎБШЮЊ1ЃК1ЃЌЪдХфЦНИУЛЏбЇЗНГЬЪНЁЃ_________
______HI+_____ H6TeO6=_____TeO2+_____Te+_____I2+_____H2O
ЃЈ3ЃЉДгДжЭОЋСЖЕФбєМЋФрЃЈжївЊКЌгаCu2TeЃЉжаЬсШЁДжэкЕФвЛжжЙЄвеСїГЬШчЯТЃК

Ђй вбжЊМгбЙЫсНўЪБПижЦШмвКЕФpHЮЊ5.0ЃЌЩњГЩTeO2ГСЕэЁЃШчЙћH2SO4ШмвКХЈЖШЙ§ДѓЃЌНЋЕМжТTeO2ГСЕэВЛЭъШЋЃЌдвђЪЧ______________ЁЃ
Ђк ЗРжЙОжВПЫсЖШЙ§ДѓЕФВйзїЗНЗЈЪЧ_____________ЁЃ
Ђл ЖдТЫдќЁАЫсНўЁБКѓЃЌНЋNa2SO3МгШыTe(SO4)2ШмвКжаНјааЁАЛЙдЁБЕУЕНЙЬЬЌэкЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧ______________ЁЃ
Ђм ЁАЛЙдЁБЕУЕНЙЬЬЌэкКѓЗжРыГіДжэкЕФЗНЗЈ_________ЃЌЖдДжэкНјааЯДЕгЃЌХаЖЯЯДЕгИЩОЛЕФЪЕбщВйзїКЭЯжЯѓЪЧ___________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПCoCl2ЁЄ6H2OЪЧвЛжжЫЧСЯгЊбјЧПЛЏМСЁЃвЛжжРћгУЫЎюмПѓ(жївЊГЩЗжЮЊCo2O3ЁЂCo(OH)3ЃЌЛЙКЌЩйСПFe2O3ЁЂAl2O3ЁЂMnOЕШ)жЦШЁCoCl2ЁЄ6H2OЕФЙЄвеСїГЬШчЯТЃК

вбжЊЃКЂйНўГівККЌгаЕФбєРызгжївЊгаH+ЁЂCo2+ЁЂFe2+ЁЂMn2+ЁЂAl3+ЕШЃЛ
ЂкВПЗжбєРызгвдЧтбѕЛЏЮяаЮЪНГСЕэЪБШмвКЕФpHМћЯТБэЃК(Н№ЪєРызгХЈЖШЮЊЃК0.01mol/L)
ГСЕэЮя | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
ПЊЪМГСЕэ | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
ЭъШЋГСЕэ | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
ЂлCoCl2ЁЄ6H2OШлЕуЮЊ86ЁцЃЌМгШШжС110~120ЁцЪБЃЌЪЇШЅНсОЇЫЎЩњГЩЮоЫЎТШЛЏюмЁЃ
ЃЈ1ЃЉаДГіНўГіЙ§ГЬжаCo2O3ЗЂЩњЗДгІЕФРызгЗНГЬЪН ЁЃ
ЃЈ2ЃЉаДГіNaClO3ЗЂЩњЗДгІЕФжївЊРызгЗНГЬЪН ЃЛШєВЛЩїЯђЁАНўГівКЁБжаМгЙ§СПNaClO3ЪБЃЌПЩФмЛсЩњГЩгаЖОЦјЬхЃЌаДГіЩњГЩИУгаЖОЦјЬхЕФРызгЗНГЬЪН ЁЃ
ЃЈ3ЃЉЁАМгNa2CO3ЕїpHжСaЁБ,Й§ТЫЫљЕУЕНЕФГСЕэГЩЗжЮЊ ЁЃ
ЃЈ4ЃЉЁАВйзї1ЁБжаАќКЌ3ИіЛљБОЪЕбщВйзїЃЌЫќУЧвРДЮЪЧ ЁЂ КЭЙ§ТЫЁЃжЦЕУЕФCoCl2ЁЄ6H2OдкКцИЩЪБашМѕбЙКцИЩЕФдвђЪЧ ЁЃ
ЃЈ5ЃЉнЭШЁМСЖдН№ЪєРызгЕФнЭШЁТЪгыpHЕФЙиЯЕШчЭМЁЃЯђЁАТЫвКЁБжаМгШынЭШЁМСЕФФПЕФЪЧ ЃЛЦфЪЙгУЕФзюМбpHЗЖЮЇЪЧ ЁЃ

AЃЎ2.0~2.5 BЃЎ3.0~3.5
CЃЎ4.0~4.5 DЃЎ5.0~5.5
ЃЈ6ЃЉЮЊВтЖЈДжВњЦЗжаCoCl2ЁЄ6H2OКЌСПЃЌГЦШЁвЛЖЈжЪСПЕФДжВњЦЗШмгкЫЎЃЌМгШызуСПAgNO3ШмвКЃЌЙ§ТЫЁЂЯДЕгЃЌНЋГСЕэКцИЩКѓГЦЦфжЪСПЁЃЭЈЙ§МЦЫуЗЂЯжДжВњЦЗжаCoCl2ЁЄ6H2OЕФжЪСПЗжЪ§Дѓгк100ЃЅЃЌЦфдвђПЩФмЪЧ ЁЃ(Д№вЛЬѕМДПЩ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаРызгЗНГЬЪНжаЃЌе§ШЗЕФЪЧЃЈ ЃЉ
A. ТШЦјИњТШЛЏбЧЬњШмвКЗДгІЩњГЩТШЛЏЬњЃКFe2++Cl2=Fe3++2Cl-
B. ЭИњЯЁЯѕЫсЗДгІЃЌВњЮяжЎвЛЪЧЯѕЫсЭЃКCu+2H+=Cu2++H2Ёќ
C. ЬМЫсЧтФЦШмвКИњДзЫсЗДгІЃКHCO3Ѓ+H+=CO2Ёќ+H2O
D. ЬМЫсИЦИњЯЁбЮЫсЗДгІЃКCaCO3+2H+=Ca2++CO2Ёќ+H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪдМСжаЃЌПЩвдМјБ№ЖўбѕЛЏЬМКЭЖўбѕЛЏСђЕФЪЧЃЈ ЃЉ
A.ГЮЧхЪЏЛвЫЎ
B.ЦЗКьШмвК
C.ЪЊШѓЕФРЖЩЋЪЏШяЪджН
D.ЯѕЫсвјШмвК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭЗлЗХШыЯЁСђЫсШмвКжаЃЌМгШШКѓЮоУїЯдБфЛЏЃЌЕЋМгШыЯТСаФГжжбЮКѓЭЗлж№НЅШмНтЃЌетжжбЮЪЧ( )
AЃЎNaCl BЃЎKNO3 CЃЎK2SO4 DЃЎNa2CO3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪГЦЗЯуОЋВЄТмѕЅЕФЩњВњТЗЯпЃЈЗДгІЬѕМўТдШЅЃЉШчЯТЃК

ЯТСаа№ЪіДэЮѓЕФЪЧ
AЃЎВНжшЃЈ1ЃЉВњЮяжаВаСєЕФБНЗгПЩгУFeCl3ШмвКМьбщ
BЃЎВНжшЃЈ2ЃЉВњЮяжаВаСєЕФЯЉБћДМПЩгУфхЫЎМьбщ
CЃЎБНЗгКЭВЄТмѕЅОљПЩгыЫсадKMnO4ШмвКЗЂЩњЗДгІ
DЃЎБНбѕввЫсКЭВЄТмѕЅОљПЩгыNaOHШмвКЗЂЩњЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃК2CO(g)+O2(g)=2CO2(g)ІЄH=-566kJЁЄmol-1 ЃЛNa2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g)ІЄH=-226 kJЁЄmol-1
ИљОнвдЩЯШШЛЏбЇЗНГЬЪНХаЖЯЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
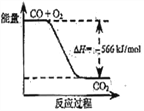
A. COЕФШМЩеШШЮЊ283 kJ
B. ЩЯЭМПЩБэЪОгЩCOЩњГЩCO2ЕФЗДгІЙ§ГЬКЭФмСПЙиЯЕ
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ІЄHЃО-452 kJЁЄmol-1
D. CO(g)гыNa2O2(s)ЗДгІЗХГі509 kJШШСПЪБЃЌЕчзгзЊвЦЪ§ЮЊ6.02ЁС1023
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЕФЖЈШнШнЦїжаЃЌЕБЯТСаФФаЉЮяРэСПВЛдйЗЂЩњБфЛЏЪБЃЌБэУїЗДгІЃК
AЃЈsЃЉ+2BЃЈgЃЉ![]() CЃЈgЃЉ+DЃЈgЃЉвбДяЕНЦНКтзДЬЌЕФЪЧЃЈ ЃЉ
CЃЈgЃЉ+DЃЈgЃЉвбДяЕНЦНКтзДЬЌЕФЪЧЃЈ ЃЉ
Ђй ЛьКЯЦјЬхЕФбЙЧПЃЛЂк ЛьКЯЦјЬхЕФУмЖШЃЛЂл BЕФЮяжЪЕФСПХЈЖШЃЛЂм ЦјЬхзмЮяжЪЕФСПЃЛЂн ЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЃЛЂо CЁЂDЗДгІЫйТЪЕФБШжЕ
A. ЂкЂлЂн B. ЂйЂкЂл C. ЂкЂлЂмЂо D. ЂйЂлЂмЂн
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com