
| A. | 酸与碱恰好完全反应生成正盐的溶液 | |
| B. | pH=7的溶液 | |
| C. | 使石蕊试液呈紫色的溶液 | |
| D. | c(H+)=c(OH-)=10-6mol•L-1的溶液 |
分析 任何溶液中当c(H+)=c(OH-)时,该溶液呈中性;如果c(H+)>c(OH-)则呈酸性,如果c(H+)<c(OH-),则呈碱性,据此分析解答.
解答 解:A.酸与碱恰好完全反应生成正盐的溶液可能呈中性,也可能呈酸性或碱性,强酸强碱盐呈中性,如NaCl溶液,强酸弱碱盐呈酸性如NH4Cl溶液,强碱弱酸盐溶液呈碱性如Na2CO3,故A错误;
B.pH=7的溶液不一定呈中性,可能呈碱性或酸性,100℃时纯水溶液的pH=6,此温度下pH=7的溶液呈碱性,故B错误;
C.常温下石蕊的变色范围是5-8,所以使石蕊试液呈紫色的溶液可能呈酸性、中性或碱性,故C错误;
D.c(H+)=c(OH-)=10-6mol•L-1的溶液中氢离子和氢氧根离子浓度相等,所以溶液呈中性,故D正确;
故选D.
点评 本题考查溶液酸碱性判断,溶液酸碱性要根据溶液中c(H+)、c(OH-)的相对大小判断,不能根据溶液的pH或溶液中的溶质判断,易错选项是B.


科目:高中化学 来源: 题型:选择题
| A. | 非金属性:F>O>S | B. | 金属性:Rb>K>Li | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴水混合后振荡,水层褪色 | |
| B. | 乙烯通入酸性KMnO4溶液中,溶液褪色 | |
| C. | CH4与Cl2的混合气体光照后颜色变浅 | |
| D. | 乙烯通入溴水中,溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下两种气体的体积之比等于物质的量之比 | |
| B. | 同温同压下两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下两种气体的摩尔质量之比等于密度之比 | |
| D. | 同温同体积下两种气体的物质的量之比等于压强之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
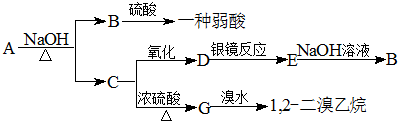
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
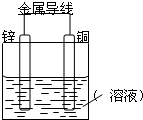 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com