
| A. | 稀有气体p区 | B. | 过渡元素d区 | C. | 副族元素ds区 | D. | 主族元素s区 |
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 在无色溶液中滴入酚酞试液 | 产生气泡 | 该溶液一定是碱溶液 |
| D | 将水蒸气通过灼热的铁粉 | 溶液变红色 | 铁与水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{adω}{24}$mol | B. | $\frac{dω}{24a}$mol | C. | $\frac{adω}{22400}$mol | D. | $\frac{adω}{12}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=b>0时,该反应达到化学平衡状态 | |
| B. | 该反应达到化学平衡状态时,一定有a>b | |
| C. | 当密闭容器内气体密度不再改变时,该反应达到化学平衡状态 | |
| D. | 密闭容器中X和Y的物质的量之比为1:2时,该反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a<2b | C. | a=b | D. | 2a=b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳棒上有气体放出,溶液pH变大 | B. | a是正极,b是负极 | ||
| C. | 电子从a极流向b极 | D. | a极上发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Na2CO3 固体中混有的少量的NaHCO3:置于坩埚中加热 | |
| B. | 除去FeCl2溶液中的FeCl3:加入铁粉 | |
| C. | 除去氢氧化铁胶体中所含的盐酸:过滤 | |
| D. | 除去CO2中混有的少量的HCl:通过饱和的NaHCO3溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
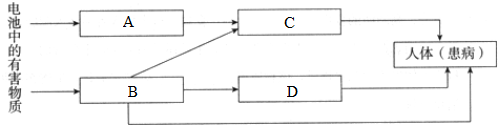
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com