
| A、Cl2 |
| B、NaCl |
| C、NH4Cl |
| D、Na2CO3 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
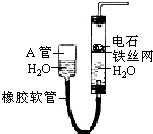 图中的实验装置可用于制取乙炔.请填空:
图中的实验装置可用于制取乙炔.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g C2H4所含共用电子对数目为4NA |
| B、1mol甲基(-CH3)所含的电子总数为7NA |
| C、标准状况下,11.2L己烷所含分子数为0.5NA |
| D、0.5mol 1,3-丁二烯分子中含有C=C双键数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2 |
| B、AgNO3 |
| C、Ba(OH)2 |
| D、H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它的单体的结构简式为:CH2=CH-COOR |
| B、它在一定条件下能发生加成反应 |
| C、它在一定条件下能发生缩聚反应 |
| D、它有固定的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质量 | B、密度 |
| C、电子总数 | D、原子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数:Y>X>Z>W |
| B、离子半径:X+>Y2+>Z->W2- |
| C、原子最外层电子数:Z>W>Y>X |
| D、还原性:X>Y W2->Z- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com