
| A£® | ¢Ś¢Ū¢Ü¢Ż | B£® | ¢Ł¢Ū¢Ü¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ü¢Ż |
·ÖĪö ±½Čē“ęŌŚĢ¼Ģ¼Ė«¼ü£¬æÉ·¢Éś¼Ó³É”¢¼Ó¾ŪŗĶŃõ»Æ·“Ó¦£¬æÉŹ¹äåĖ®”¢øßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ČēĪŖµ„Ė«¼ü½»Ģę£¬ŌņĮŚ¶ž¼×±½“ęŌŚĶ¬·ÖŅģ¹¹Ģ壬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ¢Ł±½²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ĖµĆ÷±½·Ö×ÓÖŠ²»ŗ¬Ģ¼Ģ¼Ė«¼ü£¬¹Ź¢ŁÕżČ·£»
¢Ś±½»·ÉĻĢ¼Ģ¼¼üµÄ¼ü³¤ĻąµČ£¬ĖµĆ÷±½»·½į¹¹ÖŠµÄ»Æѧ¼üÖ»ÓŠŅ»ÖÖ£¬ĖµĆ÷±½·Ö×ÓÖŠ²»“ęŌŚĢ¼Ģ¼µ„”¢Ė«¼üµÄ½»Ģę½į¹¹£¬¹Ź¢ŚÕżČ·£»
¢Ū±½ÄÜŌŚŅ»¶ØĢõ¼žĻĀøśH2¼Ó³ÉÉś³É»·¼ŗĶ飬·¢Éś¼Ó³É·“Ó¦ŹĒĖ«¼ü»ņČż¼ü¾ßÓŠµÄŠŌÖŹ£¬²»ÄÜÖ¤Ć÷±½»·½į¹¹ÖŠ²»“ęŌŚC-Cµ„¼üÓėC=CĖ«¼üµÄ½»Ģę½į¹¹£¬¹Ź¢Ū“ķĪó£»
¢ÜČē¹ū±½ŹĒµ„Ė«¼ü½»Ģę½į¹¹£¬ŌņĮŚ¶ž¼×±½µÄ½į¹¹Ó¦øĆÓŠĮ½ÖÖ£¬¶ŌÓ¦µÄ¶ž¼×±½ÓŠ4ÖÖ½į¹¹£¬¶ų¶ž¼×±½Ö»ÓŠČżÖÖ½į¹¹£¬æÉĖµĆ÷²»“ęŌŚµ„”¢Ė«¼ü½»ĢęµÄ½į¹¹£¬¹Ź¢ÜÕżČ·£»
¢Ż±½·Ö×Ó¾ßÓŠĘ½ĆęÕżĮł±ßŠĪ½į¹¹£¬ĖµĆ÷±½·Ö×ÓÖŠ²»“ęŌŚĢ¼Ģ¼µ„”¢Ė«¼üµÄ½»Ģę½į¹¹£¬¹Ź¢ŻÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģā漲鱽µÄ½į¹¹ÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦£¬ĢāÄæÄŃ¶Č²»“ó£¬ŅŖĒóÖŖŹ¶ÕĘĪÕČ«Ćę£¬ÄÜŌĖÓĆÖŖŹ¶·ÖĪöŗĶ½ā¾öĪŹĢā£¬ÖŲŌŚÄÜĮ¦µÄ漲飬עŅā±½µÄĮŚĪ»¶žŌŖČ”“śĪļÖ»ÓŠŅ»ÖÖ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½·Ö×ÓÖŠµÄ6øöĢ¼Ō×ÓÖ®¼äµÄ¼üĶźČ«ĻąĶ¬£¬ŹĒŅ»ÖÖ½éÓŚĢ¼Ģ¼µ„¼üŗĶĢ¼Ģ¼Ė«¼üÖ®¼äµÄ¶ĄĢŲµÄ¼ü | |
| B£® | Ņ»¶ØĢõ¼žĻĀ£¬Cl2æÉŌŚ¼×±½µÄ±½»·»ņ²ąĮ“ÉĻ·¢ÉśČ”“ś·“Ó¦ | |
| C£® | ŅŅĶéŗĶ±ūĻ©µÄĪļÖŹµÄĮæ¹²1 mol£¬Ęä»ģŗĻĪļĶźČ«Č¼ÉÕÉś³É3 mol H2O | |
| D£® | ½«äåĖ®¼ÓČė±½ÖŠ£¬äåĖ®µÄŃÕÉ«±äĒ³£¬ÕāŹĒÓÉÓŚ·¢ÉśĮĖ¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Į×ŌŖĖŲŹĒÉśĆüĢåÖŠÖŲŅŖµÄŌŖĖŲÖ®Ņ»
Į×ŌŖĖŲŹĒÉśĆüĢåÖŠÖŲŅŖµÄŌŖĖŲÖ®Ņ»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

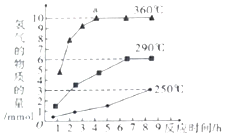
| A£® | Ķ¼1±ķŹ¾Ä³ĪüČČ·“Ó¦·Ö±šŌŚÓŠ”¢ĪŽ“߻ƼĮµÄĒéæöĻĀ·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ | |
| B£® | Ķ¼2±ķŹ¾³£ĪĀĻĀ£¬µČĮæŠæ·ŪÓė×ćĮæµÄµČÅØ¶ČµÄŃĪĖį·“Ó¦£ØµĪ¼ÓCuSO4ČÜŅŗµÄĪŖŠéĻߣ© | |
| C£® | Ķ¼3±ķŹ¾KNO3µÄČܽā¶ČĒśĻߣ¬aµćĖłŹ¾µÄČÜŅŗŹĒ80”ꏱKNO3µÄ²»±„ŗĶČÜŅŗ | |
| D£® | Ķ¼4±ķŹ¾Ė®ČÜŅŗÖŠc£ØH+£©ŗĶc£ØOH £©µÄ¹ŲĻµ£¬ŌŚĖ®ÖŠĶØŹŹĮæKClĘųĢåæÉ“Óaµć±äµ½cµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “×ĖįČÜŅŗÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH++OH-ØTH2O | |
| B£® | H2OµÄµēĄė·½³ĢŹ½£ŗH2O+H2O?H3O++OH- | |
| C£® | ¼×ĶéµÄČ¼ÉÕČČĪŖ890.3 kJ•mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4£Øg£©+2O2£Øg£©ØTCO2£Øg£©+2H2O £Øg£©”÷H=-890.3 kJ•mol-1 | |
| D£® | Ė«ŃõĖ®ÖŠ¼ÓČėĻ”ĮņĖįŗĶKIČÜŅŗ£ŗH2O2+2I-+H+ØTI2+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØA2-£©£¾c£ØH2A£© | B£® | c£ØNa+£©+c£ØH+£©=c£ØOH-£©+c£ØHA-£©+2c£ØA2-£© | ||
| C£® | c£ØNa+£©=c£Ø HA-£©+c£ØH2A£© | D£® | c£ØH+£©=c£ØA2-£©+c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2ÄÜŹ¹FeCl3”¢ĖįŠŌKMnO4ČÜŅŗŃøĖŁĶŹÉ« | |
| B£® | æÉŅŌÓĆ³ĪĒåŹÆ»ŅĖ®Ą“¼ų±šSO2ÓėCO2 | |
| C£® | °±ĘųŗĶĖįĻąÓö¶¼ÄܲśÉś°×É«ŃĢĪķ | |
| D£® | ŌŚ·“Ó¦NH3++H+=NH4+ÖŠ£¬°±Ź§Č„µē×Ó±»Ńõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com