
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
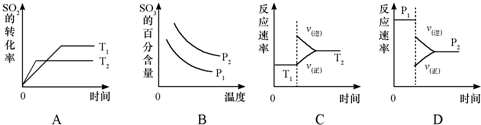
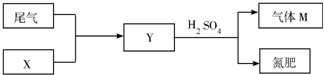
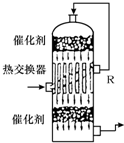 (2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题:
(2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题:
| ||
| ||
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2+2NH3+H2O![]() (NH4)2SO3
(NH4)2SO3
(NH4)2SO3+SO2+H2O![]() 2NH4HSO3
2NH4HSO3
当吸收液中NH4HSO3达到一定浓度后,再与硫酸反应。放出的SO2可循环利用,生成的(NH4)2SO4可作化肥。化学方程式是:2NH4HSO3+H2SO4![]() (NH4)2SO4+2SO2↑+2H2O
(NH4)2SO4+2SO2↑+2H2O
(NH4)2SO3+H2SO4![]() (NH4)2SO4+SO2↑+H2O
(NH4)2SO4+SO2↑+H2O
每生成1 mol(NH4)2SO4,回收SO2的体积(标准状况下)可能为( )
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制硫酸尾气中的SO2回收常采用氨吸收法。即先用氨水吸收尾气中的SO2,化学方程式为:
SO2+2NH3+H2O====(NH4)2SO3
(NH4)2SO3+SO2+H2O====2NH4HSO3
当吸收液中NH4HSO3达到一定浓度后,再与硫酸反应。放出的SO2可循环利用,生成的(NH4)2SO4可作化肥。化学方程式是:2NH4HSO3+H2SO4====(NH4)2SO4+2SO2↑+2H2O
(NH4)2SO3+H2SO4====(NH4)2SO4+SO2↑+H2O
每生成1 mol(NH4)2SO4,回收SO2的体积(标准状况下)可能为( )
A.22.4 L B.33.6 L C.44.8 L D.56 L
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com