
【题目】下列实验能达到目的的是
A. 用可见光束照射以区别溶液和胶体
B. 将NH4Cl溶液蒸干制备NH4Cl固体
C. 用萃取分液的方法除去酒精中的水
D. 只滴加氨水鉴别NaCl、A1Cl3、MgCl2、Na2SO4四种溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有____________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
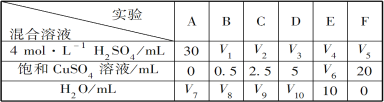
请完成此实验设计,其中:V1=___________,V6=___________,V9=___________;
反应一段时间后,实验A中的金属呈___________色,实验E中的金属呈___________色;
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用离子方程式解释以下指定反应,书写正确的是( )
A. 亚硫酸钠溶液显碱性:SO32-+2H2O=H2SO3+2OH-
B. (NH4)2FeSO4溶液与过量NaOH溶液混合制取氢氧化亚铁:Fe2++2OH-=Fe(OH)2
C. NaAlO2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-
D. 铁红溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A.K=![]()
B.K=![]()
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(原创)下列事实能用勒夏特列原理解释的是
A.使用催化剂,在单位时间内提高合成氨产率
B.对于2HI(g) ![]() H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
C.对于2CaO2(s) ![]() 2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
D.溴水中有下列平衡:Br(aq)+ H2O(l) ![]() HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关表述正确的是 ( )
A. 磷脂是所有细胞必不可少的脂质
B. 所有生物的组成成分都有DNA
C. 只有多糖、蛋白质、脂肪三类生物大分子以碳链为骨架
D. 被形容为“生命的燃料”的物质是储存能量的淀粉或糖原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组在实验室利用甲烷与氯气反应制取副产品盐酸,其设计的装置如下:
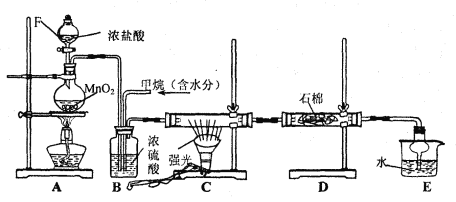
根据要求填空:
(1) 写出CH4与Cl2生成一氯代物的化学反应方程式 ;
(2) B装置有三种功能:①控制气体流速;②将气体混合均匀;③________________;
(3) D装置中的石棉上吸附着KI饱和液及KI粉末,其作用是 ;
(4) E装置的作用是____________(填编号);
A.收集气体 B.防止倒吸 C.吸收氯气 D.吸收氯化氢
(5) E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法为 。
(6) 该装置还有缺陷,原因是没有进行尾气处理,其尾气的主要成分是___________(填编号)。
A.CH3Cl B.CH2Cl2 C.CHCl3 D.CCl4 E.CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个![]() 键和1个大
键和1个大![]() 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4 -中不存在 。
A、共价键
B、非极性键
C、配位键
D、σ键
E、π键
写出一种与 CN- 互为等电子体的单质分子式 。
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于 区。
(4)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
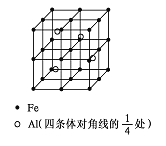
① 确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com