
(14分)己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式 ;V原子的结构示意图 ;
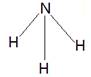
Z的氢化物结构式为 ;写出U元素在周期表中的位置
N2W2中含有的化学键的种类
(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量澄清石灰水反应的离子方程式为 。
(3)从化合价升降的角度推测UW2与V元素的单质在水溶液中反应的化学方程式是 。
(1)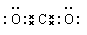 ;
;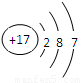 ,
,
第3周期第VIA族, 离子键和共价键 (各2分)
(2)NH4++HCO3-+Ca2++2OH-=NH3·H2O+CaCO3↓+H2O (2分)
(3)SO2+Cl2+2H2O=2HCl+H2SO4 (2分)
【解析】考查原子核外电子的排布规律及元素周期表的结构。Y原子的L层电子数是K层电子数的2倍,所以Y是碳元素。U原子的最外层电子数是其电子层数的2倍,且U的原子序数大于Y的,所以U是硫元素。常见A2B、A2B2型化合物是氧化钠、过氧化钠和水、双氧水。所以X是氢元素,W是氧元素,N是钠元素。Z的原子序数介于碳和氧之间,所以Z是氮元素。
(1)CO2是由极性键形成的共价化合物,电子式为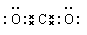 。氨气分子中含有3个极性键,结构式为
。氨气分子中含有3个极性键,结构式为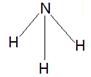 。
。
(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物是NH4HCO3,
和澄清的石灰水反应生成碳酸钙和氨水,方程式NH4++HCO3-+Ca2++2OH-=NH3·H2O+CaCO3↓+H2O
(3)SO2中的硫元素是+4价,具有还原性。氯气具有氧化性,所以能把SO2氧化生成硫酸,方
程式为SO2+Cl2+2H2O=2HCl+H2SO4。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省浙东北三校高一下学期期中联考化学试卷(带解析) 题型:填空题
(14分)己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式 ;V原子的结构示意图 ;
Z的氢化物结构式为 ;写出U元素在周期表中的位置
N2W2中含有的化学键的种类
(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量澄清石灰水反应的离子方程式为 。
(3)从化合价升降的角度推测UW2与V元素的单质在水溶液中反应的化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com