
科目:高中化学 来源:2016-2017学年陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各项操作中,能出现沉淀,且沉淀不消失的是( )
①向饱和碳酸钠溶液中通入过量的CO2;
②向NaAlO2溶液中逐滴加入过量的NaHSO4溶液;
③向AlCl3溶液中逐滴加入过量浓氨水;
④向明矾(KAl(SO4)2)溶液中逐滴加入过量的Ba(OH)2溶液;
⑤向NaAlO2溶液中逐渐通入CO2 至过量
⑥将一小块Na投入Fe2(SO4)3溶液中
A. 全部 B. ②③④⑤ C. ①③⑤⑥ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:实验题
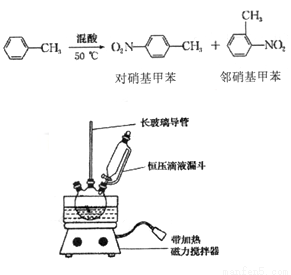
实验室制备一硝基甲笨(主要含邻硝基甲苯和对硝基甲苯)的反应原理、实验装
密度/(g·cm-3) | 沸点/℃ | 式量 | 溶解性 | |
甲苯 | 0.866 | 110.6 | 92 | 不溶于水,易溶于一硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 137 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 137 | 不溶于水,易溶于液态烃 |
实验步骤:
① 配制混酸,组装如图反应装置。取100 mL 烧杯,用10 mL 浓硫酸与30 mL 浓硝酸配
制混酸,加入恒压滴液漏斗中,把15 mL 甲苯(折合质量13.0g)加入三颈烧瓶中。
② 向室温下的甲苯中逐滴加混酸,边滴边搅拌,混合均匀。
③ 在50一60℃ 下发生反应,直至反应结束。
④ 除去混酸后,依次用蒸馏水和10% NaCO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
请回答下列问题:
(l)配制40mL 混酸的操作是________________
(2)装置中还缺少__________(填仪器名称)。如果温度超过60℃,将会有____(填物质名称)生成。
(3)分离粗产品和水的操作方法是__________
(4)产品用10% NaCO3溶液洗涤之后,再用蒸馏水洗涤,检验产品是否洗干净的操作是_______
(5)为了得到更纯净的硝基苯,还须先向液体中加入_______除去水,然后蒸馏,若最终得到产品的质量为13.70g,则一硝基甲苯的产率是________。
查看答案和解析>>
科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:选择题
短周期元素X、Y、Z、W在周期表中的相对位置如图所示,已知X原子的最外层电子数为4.下列说法不正确的是
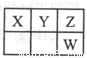
A. Z元素的常见化合价为:-1、-2
B. X元素的氢氧化物的沸点一定比Z的低
C. Y、Z、W形成的简单离子中,半径最小的是Z
D. Z元素的单质能从Na2W溶液中置换出W的单质
查看答案和解析>>
科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:选择题
下列表示正确的是
A. 含8个中子的碳原子核素符号:12C B. HF的电子式: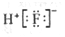
C. Cl-的结构示意图: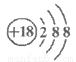 D. CH4分子的比例模型:
D. CH4分子的比例模型:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
课外活动小组探究久置的铝热剂(含Al、Al2O3、Fe2O3)的组成。称取样品3.510 g加入25.00 mL稀硫酸中,固体完全溶解,生成气体537.6 mL(标准状况),并得到溶液X。X不能使KSCN溶液变色。往X中加入过量NaOH溶液,沉淀经过滤、洗涤后,在空气中充分灼烧至恒重,冷却,称得剩余固体质量为2.400 g。下列说法一定正确的是
A. 样品中Al的物质的量为0.0160 mol
B. 样品中Al2O3的质量为0.408 g
C. 所用稀硫酸的浓度为2.64 mol·L-1
D. X中Fe2+与Al3+物质的量之比为15∶13
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二学业水平模拟测试化学试卷(解析版) 题型:选择题
N2+3H2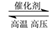 2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A. 增加N2的浓度能加快反应速率 B. 降低体系温度能加快反应速率
C. 使用催化剂不影响反应速率 D. N2足量时,H2能100%转化为NH3
查看答案和解析>>
科目:高中化学 来源:2017届山东省青岛市高三第一次统一质量检测理综化学试卷(解析版) 题型:简答题
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属。A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满。
(1)E元素的名称为________,该元素基态原子的价电子排布式为_______。
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为____(用化学式表示);原因_____。
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如下表:
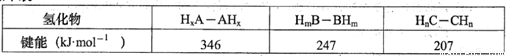
上述三种氢化物中,A、B、C元素原子的杂化方式有_____种;请解释上表中三种氢化物M-M单键的键能依次下降的原因______________________。
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式__________;该熔体中阴离子的空间构型为________。
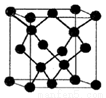
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为______(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为______g/cm3。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
一定条件下,在体积一定的密闭容器中加入1mol N2和3mol H2发生反应:N2+3H2 2NH3(正反应是放热反应).下列有关说法正确的是
2NH3(正反应是放热反应).下列有关说法正确的是
A. 升高温度能加快反应速率
B. 1mol N2和3mol H2的总能量低于2mol NH3的总能量
C. 达到化学反应限度时,生成2molNH3
D. 平衡时各组分含量之比一定等于3:1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com