
����Ŀ����ѧ�С����������װ�ã��Ʊ�LiH���塣
��1��Ԫ��������ڱ��е�λ�� __________________��
��2����LiH�����бȽ����Ӱ뾶��С��ϵr(Li+) _________r(H-)��(����>������<��)
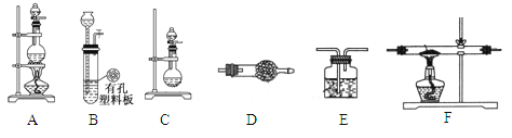
��3���С����������������װ���Ʊ�LiH���塣��ѡ�õ�ҩƷ�У�����ﮡ�п����ϡ���ᡢŨ���ᡢ��ʯ�ҡ���֪���⻯ﮣ�LiH���ڸ���Ŀ��������ȶ����ڣ���ˮ�����ܹ�����ȼ�ա����ʵ�鷽�����£�
������װ������˳��ΪB��D��F��E������ҩƷǰ����Ҫ���е�ʵ�������___________________������д������IJ���������������ҩƷ������װ��D��������____________________________��
��ͨ��һ��ʱ�����������ʯӢ�ܣ��ڼ���F����ʯӢ��֮ǰ��������е�ʵ�������_______________________________��
�ۼ���һ��ʱ���ֹͣ���ȣ�����ͨ������ȴ��Ȼ��ȡ��LiH��װ�뵪���ƿ������ڰ�������ȡ����������Ŀ����Ϊ�˱���LiH������е�ˮ�����Ӵ�������Σ�ա����LiH��ˮ��Ӧ�Ļ�ѧ����ʽ___________________________________��
��ȷ�����ƵõIJ�Ʒ0.11g����һ��������������ˮ��Ӧ���ռ�������291.2 mL���ѻ���ɱ�״���������Ʒ��LiH��Li�����ʵ���֮��Ϊ____________��
���𰸡� �ڶ�����IA�� < ����װ�õ������� ��ȥH2�е�H2O��HCl �ռ�E���ų������岢����H2���� LiH + H2O = LiOH + H2�� 6��1
����������1��Ԫ��﮵�ԭ��������3�������ڱ��е�λ���ǵڶ�����IA������2����������Ų���ͬʱ���Ӱ뾶��ԭ���������������С�������Ӱ뾶��С��ϵr(Li+)��r(H-)����3�����Ʊ�����װ�ã�����ҩƷǰ����Ҫ���е�ʵ������Ǽ���װ�õ������ԣ����ɵ������к���ˮ�������Ȼ��⣬��Ҫ��ȥ����װ��D�м�ʯ�ҵ������dz�ȥH2�е�H2O��HCl���������ǿ�ȼ�����壬����ڼ���F����ʯӢ��֮ǰ��������е�ʵ��������ռ�E���ų������岢����H2��������LiH��ˮ��Ӧ����������﮺���������Ӧ�Ļ�ѧ����ʽΪLiH+H2O��LiOH+H2��������LiH��Li�����ʵ����ֱ�Ϊxmol��ymol����
LiH+H2O=H2��+LiOH
xmol xmol
2Li+2H2O=2LiOH+H2��
ymol 0.5y mol
��8x+7y��0.11��22.4(x+0.5y)��0.2912�����x=0.012��y=0.002����LiH��Li�����ʵ���֮��Ϊ0.012mol��0.002mol=6��1��


 ̽���빮�̺��Ͽ�ѧ����������ϵ�д�
̽���빮�̺��Ͽ�ѧ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��a��b��c��Ϊ�ǽ������ʣ�d��e��Ϊ����10�����ӵĹ��ۻ�����ҷ���������ԭ�Ӹ�����d��e��fΪ���ӻ����������˵��������ǣ� �� 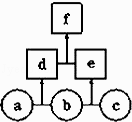
A.�����£�����a����̬
B.����c����ǿ������
C.�ȶ��ԣ�d��e
D.f�����ֽ�Ϊd��e
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���CO2��������ȡ���ͷ���ȡ��ͻ���Խ�չ��CO2ת������ʾ��ͼ���£�����˵������ȷ���ǣ�������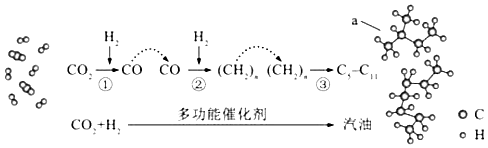
A.��Ӧ�ٵIJ����к���ˮ
B.��Ӧ����ֻ��̼̼���γ�
C.������Ҫ��C5��C11����������
D.ͼ��a��������2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ȡ����ˮ��ʵ��װ���������˵���У�����ȷ���ǣ� ��
A.���ù��˵ķ�����ȡ����ˮ
B.�������е�ˮ�������Ǵ��¿ڽ��룬�Ͽ��ų�
C.ʵ������Ҫ��������ƿ�м��뼸Ƭ���Ƭ����ֹ���ֱ�������
D.��������ƿ����ʱ�����ʯ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ�������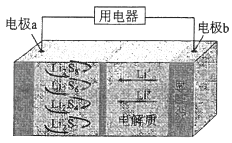
A.��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e��=3Li2S4
B.��ع���ʱ�����·������0.02 mol���ӣ��������ϼ���0.14 g
C.ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D.��س��ʱ��Խ��������е�Li2S2��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��(����)
A. ��Cl2ͨ���Ȼ�������Һ:Fe2++Cl2![]() Fe3++2Cl-
Fe3++2Cl-
B. ����ͨ��ˮ��:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C. FeCl3��Һ��ͨ������İ�ˮ: Fe3++3OH-![]() Fe(OH)3��
Fe(OH)3��
D. Cl2ͨ���ռ���Һ��:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڼ��������ܺͼ��ǣ�����˵������ȷ���ǣ� ��
A.������������������ṹ����Ҫ����
B.�����Ĵ�С��ɼ�ԭ�ӵİ뾶�ͳɼ���Ŀ�й�
C.����Խ����Խ�������ۻ�����Խ�ȶ�
D.���ǵĴ�С����������ܵĴ�С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z�����ڱ��е�λ�ù�ϵ��ͼ��ʾ����֪X����������Ϊ2����������������ȷ����
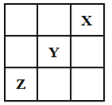
A. Y���⻯���ȶ��Դ���Z���⻯���ȶ���
B. Zһ���ǻ��õĽ���Ԫ��
C. Y������������ˮ������һ��ǿ��
D. 1molX�ĵ��ʿ��Ը�����ˮ��Ӧ��ת�Ƶĵ���Ϊ2mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com