
| A. | 每个分子中都含有氮分子 | B. | 每个分子中的氮原子个数相等 | ||
| C. | 每种物质中氮元素的质量分数相同 | D. | 都属于氧化物 |
分析 A.只有氮气由氮分子构成;
B.1个N2、N2O、N2O5中均含2个N原子;
C.氮气中N元素质量分数为100%,而N2O、N2O5中均含O元素;
D.氧化物一定含两种元素、且含氧元素.
解答 解:A.只有氮气由氮分子构成,而N2O、N2O5不含氮分子,故A错误;
B.1个N2、N2O、N2O5中均含2个N原子,则每个分子中的氮原子个数相等,故B正确;
C.氮气中N元素质量分数为100%,而N2O、N2O5中均含O元素,含O原子越多时N的质量分数越低,则每种物质中氮元素的质量分数不相同,故C错误;
D.氧化物一定含两种元素、且含氧元素,则氮气为单质,只有N2O、N2O5为氧化物,故D错误;
故选B.
点评 本题考查含氮物质,为高频考点,把握物质的组成、构成、氧化物及质量分数为解答的关键,侧重分析与应用能力的考查,注重基础知识的夯实,题目难度不大.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | <1:1 | C. | ≥1:1 | D. | 任意比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入少量 HCl 气体 | B. | 加入少量 NaOH 固体 | ||
| C. | 加入少量 H2O | D. | 适当升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液 | B. | 硫酸氢钠溶液 | C. | 硫酸钾溶液 | D. | 硝酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠在研体中研成粉末,使钠与水反应的实验更安全 | |
| B. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| C. | 分液时,分液漏斗内的上层液体应由上口倒出 | |
| D. | 用滴定管取液时,开始和最后读数时均俯视,则量取的体积准确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
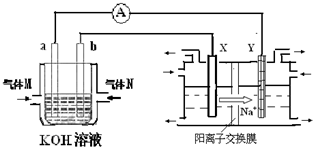
| 时间(h) 物质的量/(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com