
分析 在CH3COONa溶液中,OH-全部来自于水的电离,结合溶液中离子积常数计算水电离出的氢离子浓度判断;溶液中pH=-lgc(H+),而在酸溶液中,氢离子几乎全部来自于酸的电离,但氢氧根全部来自于水的电离,而水电离出的c(H+)等于溶液中c(OH-),据此分析;
解答 解:在CH3COONa溶液中,OH-全部来自于水的电离,由于溶液的pH=11,故溶液中的氢离子浓度为10-11mol/L,由水电离出来的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-11}}$=1.0×10-3 mol•L-1;
pH等于3的CH3COOH溶液中C(H+)=1.0×10-3mol/L,25℃时:Kw=c(OH-)×c(H+)=10-14,溶液中的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-3}}$=1.0×10-11mol/L,而在酸溶液中,氢离子几乎全部来自于酸的电离,但氢氧根全部来自于水的电离,故由水电离出的C(H+)=c(OH-)=1.0×10-11mol/L,
故答案为:1.0×10-3 mol•L-1;1.0×10-11mol/L.
点评 本题考查盐溶液中和酸溶液中的来自于水的氢离子浓度的计算,正确理解混合溶液pH计算的方法等即可解答,会正确计算盐溶液中水电离出c(H+),为易错点.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③⑤ | C. | ①④ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、CCl4、酒精可用来萃取溴水中的溴 | |
| B. | 用激光笔鉴别Fe(OH)3胶体和FeCl3溶液 | |
| C. | 加入盐酸以除去硫酸钠中的少量碳酸钠杂质 | |
| D. | 在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
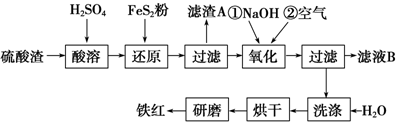
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
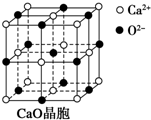 可以由下列反应合成三聚氰胺:
可以由下列反应合成三聚氰胺: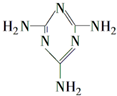 俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸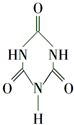 后,三聚氰酸与三聚氰胺分子相互之间通过C结合,在肾脏内易形成结石.
后,三聚氰酸与三聚氰胺分子相互之间通过C结合,在肾脏内易形成结石.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com