
| A. | 工业上用水吸收NO2生产硝酸:3NO2+H2O=2HNO3+NO | |
| B. | 用熟石灰处理泄漏的液氯:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O | |
| C. | Cu与稀硝酸反应制取硝酸铜:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| D. | 用明矾除去水中的悬浮颗粒物:Al3++3H2O?Al(OH)3(胶体)+3H+ |
分析 A.二氧化氮与水反应生成一氧化氮和硝酸;
B.氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水;
C.不符合反应客观事实;
D.铝离子水解生成氢氧化铝胶体,具有吸附性,能够吸附水中杂质颗粒.
解答 解:A.工业上用水吸收NO2生产硝酸和一氧化氮、水方程式:3NO2+H2O=2HNO3+NO,故A正确;
B.用熟石灰处理泄漏的液氯,反应的化学方程式:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,故B正确;
C.Cu与稀硝酸反应生成一氧化氮和水、硝酸铜:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故C错误;
D.用明矾除去水中的悬浮颗粒物,离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+,故D正确;
故选:C.
点评 本题考查了化学方程式、离子方程式的书写,明确反应实质是解题关键,注意离子方程式书写方法,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子中三个碳原子在同一条直线上 | |
| B. | 丙烯可使酸性高锰酸钾溶液褪色 | |
| C. | 丙烯可使溴水褪色 | |
| D. | 丙烯能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  |  | 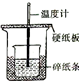 |
| A.测量锌与稀硫酸反应的速率 | B.构造铜锌原电池 | C.进行酸碱中和滴定实验 | D.测定中和热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
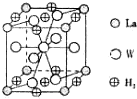 有A、B、C、D、E、F、G、W八种原子序数依次增大的元素(原子序数均小于30),A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,E、F同主族,G与W同周期同族且原子序数相差2.请回答下列问题:
有A、B、C、D、E、F、G、W八种原子序数依次增大的元素(原子序数均小于30),A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,E、F同主族,G与W同周期同族且原子序数相差2.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.
第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途.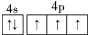 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 和高分子化合物PCL的合成路线如下:
和高分子化合物PCL的合成路线如下:
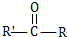 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ (R、R′代表烃基)
(R、R′代表烃基)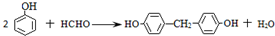 .
. .
.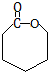 .高分子化合物PCL的结构简式是
.高分子化合物PCL的结构简式是 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Y | U | |||
| X | V | W |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水和二氧化硫都具有漂白作用,两者漂白原理相同 | |
| B. | 等质量的铜粉按a、b两种途径完全转化,途径a和途径b消耗的H2SO4相等 途径a:Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4;途径b:Cu$\stackrel{浓H_{2}SO_{4}}{→}$CuSO4 | |
| C. | 用金属钠可区分乙醇和乙醚 | |
| D. | 从海水中提取物质都必须通过化学反应才能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实 验 序 号 | 时间(min) 浓度(mol•L-1) 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A. | 该反应是吸热反应,升温正、逆反应速率增大 | |
| B. | 实验3中 c3=1.2 mol•L-1 | |
| C. | 实验1与实验3比较,A的平衡转化率之比为1:2 | |
| D. | 实验2使用了催化剂,在0至10 min内平均速率υ(B)=0.02 mol•L-1•min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com