
下列变化按氮元素只被氧化、只被还原、既不被氧化又不被还原、既可能被氧化又可能被还原的顺序排列正确的是( )
①高能固氮 ②硝酸分解 ③实验室制取氨气 ④氨氮废水脱氮(指将NH3或NH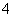 转化为N2)
转化为N2)
A.④②③① B.②①③④
C.③④②① D.③①④②
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
已知:
2Zns)+O2g)===2ZnOs) ΔH=-701.0 kJ·mol-1
2Hgl)+O2g)===2HgOs) ΔH=-181.6 kJ·mol-1
则反应Zns)+HgOs)===ZnOs)+Hgl)的ΔH为 )。
A.+519.4 kJ·mol-1 B.+259.7 kJ·mol-1
C.-259.7 kJ·mol-1 D.-519.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中存在2NO+O2 2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是( )
2NO2反应,平衡时NO的转化率与温度变化关系如图所示(曲线上任何一点都表示平衡状态),下列说法中正确的是( )
A.该反应的正反应是吸热反应。
 B.若温度为T1、T3时的平衡常数分别为K1、K3, 则K1<K3。
B.若温度为T1、T3时的平衡常数分别为K1、K3, 则K1<K3。
C.T1时,当反应处于D点,则该反应的逆反应速率
大于正反应速率。
D.如果缩小容器体积,则平衡时表示NO转化率与温度变化关系的
曲线在原曲线上方。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、101 kPa下,ΔH=-113 kJ·mol-1、ΔS=-145 J·mol-1·K-1。下列说法中错误的是( )
A.该反应中反应物的总能量高于生成物的总能量
B.该反应常温下不能自发进行,因此需要高温和催化剂
C.该反应常温下能自发进行,高温和催化剂只是加快反应的速率
D.汽车尾气中的这两种气体会与血红蛋白结合而使人中毒
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应的规律
(1)下列粒子既有氧化性又有还原性的是________。
①Fe2+ ②SO2 ③Fe ④Cl2 ⑤H2O2 ⑥HCl
⑦Fe3+ ⑧HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
黄铜矿(CuFeS2)常用于提炼金属铜。黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为2CuFeS2+O2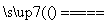
 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )
A.方框中的物质应为Cu2S
B.该反应的部分产物可用于硫酸工业
C.反应中SO2既是氧化产物又是还原产物
D.反应中若有1 mol SO2生成,则一定有4 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
向100 mL FeI2溶液中逐渐通入Cl2,会依次生成I2、Fe3+、IO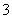 ,其中Fe3+、I2的物质的量随通入Cl2的物质的量n(Cl2)的变化如图所示,下列说法不正确的是(双选)( )
,其中Fe3+、I2的物质的量随通入Cl2的物质的量n(Cl2)的变化如图所示,下列说法不正确的是(双选)( )
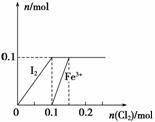
A.氧化性强弱:I2<Fe3+<IO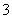
B.n(Cl2)=0.12 mol时,溶液中的离子主要有:Fe2+、Fe3+
C.若n(Cl2)∶n(FeI2)=6∶5,反应的离子方程式为2Fe2++10I-+6Cl2===5I2+2Fe3++12Cl-
D.若n(Cl2)∶n(FeI2)=2∶1,反应的离子方程式为2Fe2++4I-+3Cl2===2I2+2Fe3++6Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
能够充分说明在恒温恒容下的密闭容器中,反应2SO2(g)+O2(g) 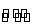
2SO3(g)已达平衡状态的标志是( )
A.容器中SO2、O2、SO3的物质的量之比为2∶1∶2
B.SO2和SO3的物质的量浓度相等
C.反应容器内压强不随时间变化而变化
D.单位时间内生成2 mol SO3的同时生成1 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
在可逆反应中,平衡常数与反应进行的限度的关系正确的是( )
A.K越大,反应程度越大
B.K越大,反应程度越小
C.K的大小与反应程度无关
D.升高温度,K增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com