
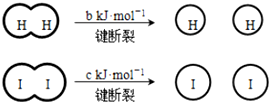
 ��a��b��c�������㣩 ����˵������ȷ���ǣ�������
��a��b��c�������㣩 ����˵������ȷ���ǣ�������| A�� | ��Ӧ�������������������������� | |
| B�� | �Ͽ� 1 mol H-H ����1 mol I-I�������������ڶϿ� 2 mol H-I���������� | |
| C�� | �Ͽ� 2 mol H-I����������ԼΪ��c+b+a�� kJ | |
| D�� | ���ܱ������м���2 mol H2��2 mol I2����ַ�Ӧ��ų�������С�� 2a kJ |
���� A���÷�Ӧ�ġ�H=-a kJ/mol��0����Ϊ���ȷ�Ӧ����������غ������
B�����ѻ�ѧ�������������γɻ�ѧ���ų���������Ϸ�Ӧ�Ƿ��ȷ�Ӧ�����жϣ�
C�������ʱ�=��Ӧ����ѻ�ѧ����Ҫ������-�������γɻ�ѧ���ų������������жϣ�
D����Ӧ�ǿ��淴Ӧ���ܽ��г��ף�
��� �⣺A��H2��I2��һ���������ܷ�����ӦΪ��H2��g��+I2��g��?2HI��g����H=-a kJ•mol-1 ���÷�ӦΪ���ȷ�Ӧ����Ӧ������������������������������A��ȷ��
B�����ѻ�ѧ�������������γɻ�ѧ���ų���������Ӧ�Ƿ��ȷ�Ӧ�����γɻ�ѧ���ų����������ڶ��ѻ�ѧ�����յ���������Ͽ�1mol H-H����1mol I-I����������С�ڶϿ�2mol H-I��������������B����
C����H=��Ӧ����ѻ�ѧ����Ҫ������-�������γɻ�ѧ���ų�������=bKJ/mol+cKJ/mol-2H-I=-akJ/mol���õ��Ͽ�2mol H-I����������ԼΪ��a+b+c��kJ����C��ȷ��
D����Ӧ�ǿ��淴Ӧ���ܽ��г��ף������ʱ�������������ܱ������м���2mol H2��2mol I2����ַ�Ӧ��ų�������С��2a kJ����D��ȷ��
��ѡB��
���� ���⿼�鷴Ӧ�����ʱ��Ӧ�ã���Ŀ�ѶȲ�����ȷ��ѧ���������ʱ�Ĺ�ϵΪ���ؼ���ע�����շ�Ӧ�����ʱ�Ĺ�ϵ��������ؿ���ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4L HF�к��з�ԭ����ĿΪNA | |
| B�� | 0.1mol/L��NH4HSO4��Һ�еμ�0.1mol/L��Ba��OH��2��Һ�������պ���ȫ��c��NH4+����c��OH-����c��SO42-����c��H+�� | |
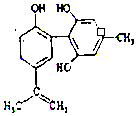
| C�� | 1mol ��ͼ������Ũ��ˮ��Ӧʱͨ���������Br2Ϊ6mol | |
| D�� | 12gʯīϩ������ʯī���к�����Ԫ���ĸ���Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
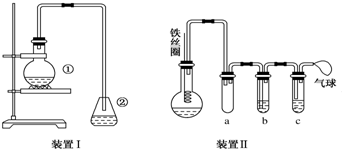
 ���������ӷ���ʽΪBr-+Ag+�TAgBr����
���������ӷ���ʽΪBr-+Ag+�TAgBr���� ��Br2��Ҫ��õ������IJ������NaOH��Һ�Լ�ϴ�ӣ�ϴ�Ӻ����ֲ�ƷӦʹ�õ������Ƿ�Һ©����
��Br2��Ҫ��õ������IJ������NaOH��Һ�Լ�ϴ�ӣ�ϴ�Ӻ����ֲ�ƷӦʹ�õ������Ƿ�Һ©�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
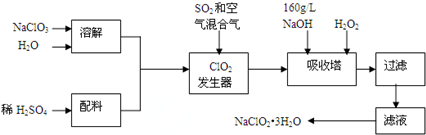
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
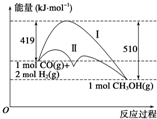 ���ú�̼������ϳ�ȼ���ǽ����ԴΣ������Ҫ��������֪CO��g��+2H2��g��?CH3OH��g����Ӧ�����е������仯�����ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ���ǣ�������
���ú�̼������ϳ�ȼ���ǽ����ԴΣ������Ҫ��������֪CO��g��+2H2��g��?CH3OH��g����Ӧ�����е������仯�����ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ���ǣ�������| A�� | �÷�Ӧ�ġ�H=+91 kJ•mol-1 | |
| B�� | ����������÷�Ӧ�ġ�H��С | |
| C�� | ��Ӧ���������С��������������� | |
| D�� | ����÷�Ӧ����Һ̬CH3OH�����H��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ���ܷ����Ĺ��̶��Ƿ��Է����� | |
| B�� | ��ϵ��������Խ�ߣ������Ҷ�Խ�ߣ���ֵ��Խ�� | |
| C�� | �����Է����еĻ�ѧ��Ӧ���Ƿ��ȷ�Ӧ | |
| D�� | ͬһ���ʵĹ̡�Һ��������״̬����ֵ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪2C��s��+O2��g��=2CO��g����H=-221 kJ•mol-1�����֪C�ı�ȼ����Ϊ110.5 kJ•mol-1 | |
| B�� | ��101KPa�������ı�ȼ���ȡ�H=-285.5 kJ•mol-1����ˮ�ֽ���Ȼ�ѧ����ʽ��2H2O��l��=2H2��g��+O2��g����H=+285.5 kJ•mol-1 | |
| C�� | ϡ������0.1 mol/LNaOH��Һ��Ӧ��H+��aq��+OH-��aq��=H2O��l����H=-57.3 kJ•mol-1 | |
| D�� | �ܱ������У�9.6 g�����11.2 g���ۻ�ϼ�������������17.6 gʱ���ų�19.12 kJ��������Fe��s��+S��g��=FeS��s����H=-95.6 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com