
 两种气体通入密闭容器中,反应按
两种气体通入密闭容器中,反应按 =
=  进行,
进行, ,
, ,
, ,则x、y的值分别为( )
,则x、y的值分别为( )| A.3和2 | B.1和3 | C.3和1 | D.4和5 |
科目:高中化学 来源:不详 题型:单选题
 2C(g)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
2C(g)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )| A.用物质A表示的反应平均速率为0.3 mol·L-1·s-1 |
| B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1 |
| C.2s时物质A的转化率为70% |
| D.2s时物质B的浓度为0.7 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Ag2O(s)+SO3(g),2 SO3(g)
Ag2O(s)+SO3(g),2 SO3(g)  2 SO2(g)+ O2(g),反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是( )
2 SO2(g)+ O2(g),反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是( )| A.这10 min内氧气的平均反应速率为0.005 mol·mol-1·min-1 |
| B.SO3的分解率为20% |
| C.容器里气体的密度为40g/L |
| D.硫酸银与三氧化硫的化学反应速率相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| l | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )
2SO3,已知V(SO2)==0.05mol·l-1·min-1,则2min后SO3的浓度为( )| A.1mol·l-1 | B.0.1mol·l-1 | C.0.9mol·l-1 | D.0.2mol·l-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大 |
| C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快 |
| D.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-= Cl2 ↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 和
和 由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。 CO(g) +3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
CO(g) +3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。 分别为
分别为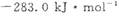 和
和 ,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。 CH3OH (g), △H<0合成甲醇,在230°C?270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
CH3OH (g), △H<0合成甲醇,在230°C?270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | N2 | 1.00 | 1.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com