
|
把50 mL 2 mol/L的NaOH溶液、100 mL 1 mol/L的H2SO4溶液、AA是反应物以及40 mL 3 mol/L的氨水混合,所得溶液能使酚酞试液呈浅红色,则溶液中离子浓度关系正确的是 | |
| [ ] | |
A. |
c( |
B. |
c(NH4+)>c( |
C. |
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)> c(H+) |
D. |
c(Na+)+c(NH4+)+c(H+)=c(OH-)+c(SO42-) |
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:阅读理解

| 滴定 次数 |
量取KMnO4溶液的体积(mL) | 标准草酸溶液的体积 | 平均值 (mL) | ||
| 滴定前刻度 | 滴定后刻度 | 实际体积(mL) | |||
| 第一次 | 5.00 | 0.00 | 19.60 | ||
| 第二次 | 5.00 | 0.20 | 19.60 | ||
| 第三次 | 5.00 | 0.06 | 18.06 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)我国首创以E(单质)—(空气,海水)—石墨(C)电池为能源的新型海水标志灯。该灯以海水为电解质溶液,靠空气中的氧气使E(单质)不断氧化而产生电流。只要把灯放入海水中数分钟,就会发出耀眼的白光,其能量比干电池高20—50倍。该电池的正极反应式是________________________________________________。
(2)将过量气体AF通入AgNO3溶液中得到白色沉淀,将此白色沉淀分成4等份并分别溶于下列物质中:①10 mL水 ②10 mL 0.1 mol·L-1的NaCl溶液 ③10 mL 0.1 mol·L-1的MgCl2溶液 ④10 mL 0.1 mol·L-1的KI溶液。则所得溶液中剩余白色固体质量由大到小的顺序为(填序号)________________________________________________。
(3)已知:
B2(g)+
B2(g)+
试写出BA3与C2反应生成BC2和A
(4)3 mol A的单质与1 mol B的单质在一个体积恒定的密闭容器中反应,生成化合物M,达到平衡时,M的体积分数为m。若将a mol A的单质、b mol B的单质、c mol M同时置于上述容器中,在相同温度下反应,达到平衡时,M的体积分数仍为m,则a、b、c必须满足的关系是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源:专项题 题型:实验题
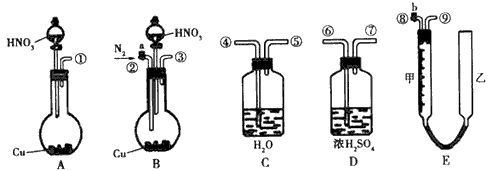
查看答案和解析>>
科目:高中化学 来源: 题型:
把下列四种X溶液分别加入四个盛有10 m L 2 mol/L盐酸的烧杯中,均加水稀释到50 mL,此时X和盐酸和缓地进行反应。其中反应速率最大的是
A、20 mL 3mol/L 的X溶液
B、20 mL 2mol/L 的X溶液
C、10 mL 4mol/L 的X溶液
D、10 mL 2mol/L 的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
把下列四种X溶液分别加入四个盛有10 m L 2 mol/L盐酸的烧杯中,均加水稀释到50 mL,此时X和盐酸和缓地进行反应。其中反应速率最大的是( )
A、20 mL 3mol/L 的X溶液 B、20 mL 2mol/L 的X溶液
C、10 mL 4mol/L 的X溶液 D、10 mL 2mol/L 的X溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com