
【题目】下图是由1~18号元素中部分元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)

请回答下列问题:
(1)物质A的化学式为____,其阴、阳离子个数比为____。
(2)化合物E溶于水中的电离方程式为____。
(3)实验室将物质C通常保存在____中,请写出反应①的离子方程式,并用单线桥标出电子转移的方向和数目____。
(4)反应②的化学方程式为____。
(5)有两个分别装有H和I固体的试剂瓶,因标签脱落而无法区分。若让你鉴别它们,下列试剂或方法中可选用的有____。
A 澄清石灰水 B 稀盐酸 C 加热,称重 D 焰色反应
【答案】Na2O2 1:2 NaOH=Na++OH- 煤油或石蜡 ![]() NaHCO3+NaOH=Na2CO3+H2O BC
NaHCO3+NaOH=Na2CO3+H2O BC
【解析】
A是由单质C在D中燃烧生成的淡黄色固体,应为Na2O2,B是最常见的无色液体,应为H2O,则D为O2,可推知,E为NaOH,C为Na,F为H2,由转化关系可知K为CO2,H为Na2CO3,I为NaHCO3,结合物质的性质和题目的要求可解答该题。
(1)A是由单质C在D中燃烧生成的淡黄色固体,应为Na2O2,其阴、阳离子个数比为1:2;
(2)由分析可知E为NaOH,电离方程式为:NaOH=Na++OH-;
(3)C为Na,实验室将物质C通常保存在煤油或石蜡中,反应①为钠和水的反应,用单线桥标出电子转移的方向和数目为:![]() ;
;
(4)由分析可知H为Na2CO3,I为NaHCO3,碳酸氢钠加氢氧化钠可变为碳酸钠,方程式为:NaHCO3+NaOH=Na2CO3+H2O;
(5)由分析可知H为Na2CO3,I为NaHCO3,
A、Na2CO3和NaHCO3都能与澄清石灰水反应生成沉淀,无法鉴别,故A错误;
B、Na2CO3和NaHCO3都能与盐酸发生反应产生气体,盐酸少量时,Na2CO3不产生气体,故B正确;
C、NaHCO3不稳定,加热易分解,质量减轻,Na2CO3不会,故C正确;
D、碳酸钠和碳酸氢钠都含有钠离子,二者焰色反应的火焰颜色相同,无法鉴别,故D错误;
正确答案是BC。


科目:高中化学 来源: 题型:
【题目】(1)19g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是__________________,A的相对原子质量是______________。
(2)1.5mol CO2中含_____ mol碳原子,________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L。
① 实验室利用石灰石制备CO2______________________________________________
② SO2和足量NaOH反应 __________________________________________________
③写一个置换反应方程式 ______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥标明该反应中电子的转移及数目:___。
(2)还原剂是___;还原产物是___;被还原与未被还原N的个数比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于氧化还原反应的是( )
A.3Cl2+6KOH=5KCl+KClO3+3H2OB.Ca(OH)2+CO2=CaCO3↓+H2O
C.Cl2+H2O ![]() HCl+HClOD.5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O
HCl+HClOD.5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3的混合溶液中滴加0.2mol·L-1稀盐酸,生成CO2的物质的量与加入盐酸的体积(V L)的关系如图所示。下列说法正确的是
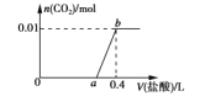
A.在0~a范围内,只发生中和反应
B.ab段发生反应的离子方程式为CO32-+2H+=CO2↑+H2O
C.a=0.3
D.原混合溶液中NaOH与Na2CO3的物质的量之比为6:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述正确的是
①常温下64 g S4和S8混合物中含有原子数为2NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤足量铁在1mol氯气中加热反应,铁失去的电子数为3NA
⑥常温常压下,17g甲基(-14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A. ①③⑤⑦B. ①②④⑧C. ②③⑥⑧D. ①②⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质的实验装置。其中D瓶中放有干燥的红色布条;E中为铜网,E右端出气管口附近为棉球。试回答:
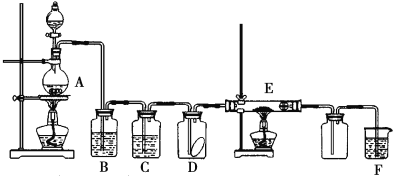
(1)A中发生反应的化学方程式为____,若产生的氯气在标准状况下的体积为22.4L,则被氧化的HCl的质量为____。
(2)为得到干燥纯净的氯气,一般B中盛放的试剂为____, C中盛放的试剂为____。
(3)E中所发生反应的化学方程式为____。
(4)F装置的作用是____,其反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是

A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com