
【题目】世界能源消费依靠化学技术,作为燃料的H2通常来自水煤气。回答下列问题:
(1)己知:① C(s)+H2O(g)=CO(g)+H2(g)△H=akJ/mol②2C(s)+O2(g)=2CO(g) △H= -220 kJ/mol③2H2O(g)=2H2(g)+O2(g) △H=+480 kJ/mol,则 a=_____kJ/mol。
(2)某实验小组在实验室模拟反应C(s) +H2O (g)![]() CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
a. v逆(H2O)=v正(CO) b.容器中物质的总质量不发生变化
c. n (H2O):n (H2)=1:1且不再改变 d.恒容容器中混合气体密度不变
(3)一定温度下,在2L盛有足量炭粉的恒容密闭容器中通入0.8molH2O发生反应①,6min时生成0.7 gH2则6 min内以CO表示的平均反应速率为 ______mol/Lmin-1 (保留2位有效数字)。
(4)燃料气中CO需氧化为CO2与氢气进行分离,使用CuO/CeO2做催化剂,并向其中加入不同的酸(HIO3 或H3PO4)后,CO的转化率随温度的变化如图所示。
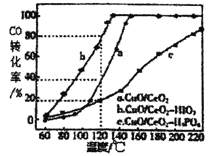
①加入H3PO4__________(填“促进”或,抑制”)CuO/CeO2的催化。
②CeO2可由草酸鋪[Ce2(C2O4)3]在空气中灼烧制备,同时只产生一种气体,写出该反应的化学方程式_____。
③恒温恒压下,在温度为120°C,催化剂为CuO/CeO2HIO3条件下反应,若起始时燃料气流速为1800mLmin-1,其中CO的体积分数为0.68%,则反应0.5h后剩余气体中CO的体积为__mL。
(5)有人将合成氨反应设计成原电池,装置如图所示。
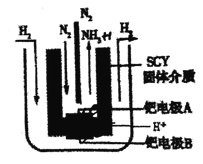
①正极反应式为 _______。
②己知该原电池的标准电动势![]() ,25°C时反应的平衡常数K与
,25°C时反应的平衡常数K与![]() 之间的关系为
之间的关系为![]() (n为原电池反应转移的电子数),则合成氨反应(N2 +3H2
(n为原电池反应转移的电子数),则合成氨反应(N2 +3H2![]() 2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
【答案】+130 acd 0.029 抑制 Ce2(C2O4)3+2O2 ![]() 2CeO2+6CO2 73.44 N2+6e-+6H+═2NH3
2CeO2+6CO2 73.44 N2+6e-+6H+═2NH3 ![]()
【解析】
(1)已知:②2C(s)+O2(g)═2CO(g) △H=-220kJmol-1,③2H2O(g)=2H2(g)+O2(g) △H=+480 kJ/mol,可利用盖斯定律,将![]() 得到①C(s)+H2O(g)═CO(g)+H2(g)的反应热,以此解答该题;
得到①C(s)+H2O(g)═CO(g)+H2(g)的反应热,以此解答该题;
(2)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3) 反应速率v=![]() ;
;
(4)①根据CO的转化率随温度的变化图分析;
②灼烧草酸铈[Ce2(C2O4)3],分解制得CeO2、一氧化碳以及二氧化碳,配平方程式即可;③温度为120℃,催化剂为CuO/CeO2-HIO3时,CO的转化率是80%,结合通入CO总体积计算;
(5)①原电池的正极发生还原反应,N2得电子还原生成NH3。
②己知N2 +3H2![]() 2NH3反应中转移电子数为6e-,原电池的标准电动势
2NH3反应中转移电子数为6e-,原电池的标准电动势![]() ,再结合
,再结合![]() 计算此反应的平衡常数K。
计算此反应的平衡常数K。
(1)已知:②2C(s)+O2(g)═2CO(g) △H=-220kJmol-1,③2H2O(g)=2H2(g)+O2(g) △H=+480 kJ/mol,可利用盖斯定律,将![]() 得到①C(s)+H2O(g)═CO(g)+H2(g),则△H=akJ/mol=
得到①C(s)+H2O(g)═CO(g)+H2(g),则△H=akJ/mol=![]() ×[(-220kJmol-1)+(+480 kJ/mol)]=+130 kJ/mol,即a=+130;
×[(-220kJmol-1)+(+480 kJ/mol)]=+130 kJ/mol,即a=+130;
(2)a.v逆(H2O)=v正(CO),达到平衡状态,故a正确;
b.容器中物质的总质量一直不发生变化,不能说明达平衡状态,故b错误;
c.n (H2O):n (H2)=1:1且不再改变,说明n(H2O)和n(H2)的物质的量一定,此时反应达到平衡状态,故c正确;
d.混合气体的体积不变,但混合气体的总质量不确定,当密度不变,则说明混合气体的总质量不再发生变化,说明达平衡状态,故d正确;
故答案为acd;
(3) 一定温度下,在2L盛有足量炭粉的恒容密闭容器中通入0.8molH2O,6min时生成0.7gH2,其物质的量为![]() =0.35mol,由C(s) +H2O (g)
=0.35mol,由C(s) +H2O (g)![]() CO (g) +H2 (g)反应可知生成CO的物质的量为0.35mol,则6min内以CO表示的平均反应速率=
CO (g) +H2 (g)反应可知生成CO的物质的量为0.35mol,则6min内以CO表示的平均反应速率= 0.029mol/(Lmin);
0.029mol/(Lmin);
(4)①图示可知,相同温度下,在CuO/CeO2催化剂中加入H3PO4时CO的转化率最低,说明加人H3PO4抑制CuO/CeO2的催化;
②灼烧草酸铈[Ce2(C2O4)3],分解制得CeO2![]() 2CeO2+4CO↑+2CO2↑;
2CeO2+4CO↑+2CO2↑;
③温度为120℃,催化剂为CuO/CeO2-HIO3时,CO的转化率是80%,若燃料气流速为1800mLmin-1,CO的体积分数为0.68%,则反应0.5小时后CO的体积为1800mLmin-1×0.5h×60min/h×0.68%×(1-80%)=73.44ml;
(5)①原电池的正极发生还原反应,N2得电子还原生成NH3,则正极反应式为N2+6e-+6H+═2NH3;
②己知N2 +3H2![]() 2NH3反应中转移电子数为6e-,原电池的标准电动势
2NH3反应中转移电子数为6e-,原电池的标准电动势![]() ,再结合
,再结合![]() ,则平衡常数K=
,则平衡常数K=![]() 。
。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】《本草图经》中关于绿矾的分解有如下描述:“绿矾形似朴消(Na2SO4·10H2O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也。”对此段话的说明中肯定错误的是( )
A. 绿矾的化学式为FeSO4·7H2O B. 绿矾分解过程中没有发生电子的转移
C. “色赤”物质可能是Fe2O3 D. 流出的液体中可能含有硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝苯地平H是一种治疗高血压的药物;其一种合成路线如下:

已知:酯分子中的a-碳原子上的氢比较活泼,使酯与酯之间能发生缩合反应。
![]()
回答下列问题:
(1)B的化学名称为________.
(2)②的反应类型是________.
(3)D的结构简式为________.
(4)H的分子式为________.
(5)反应①的化学方程式为________.
(6)已知M与G互为同分异构体,M在一定条体下能发生银镜反应,核磁共振氢谱显示有4组峰,峰面积之比为1:1:2:4,写出M的一种可能的结构简式________.
(7)拉西地平 也是一种治疗高血压药物,设以乙醇和
也是一种治疗高血压药物,设以乙醇和 为原料制备拉西地平的合成路线(无机试剂任选)。________________________
为原料制备拉西地平的合成路线(无机试剂任选)。________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】八种短周期元素原子半径的相对大小、最高正价或最低负价如图所示,下列说法错误的是()
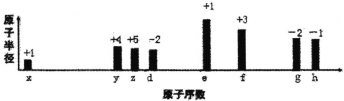
A.常见的离子半径:g>h>d>e
B.氢化物的沸点y 一定低于z
C.由d、e、g三种元素组成的盐和稀硫酸反应可能生成沉淀
D.e、f、h的最高价氧化物的水化物之间可两两反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,体积为VL两容器分别充满了CO气体和CO2气体,下列有关说法不正确的是( )
A.两容器含有气体分子数目相同
B.两容器气体密度之比为:7:11
C.两容器中所含氧原子个数之比为:1:2
D.两容器所含气体的物质的量均为:![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市售盐酸试剂瓶标签上的部分信息如下:
盐酸
分子式:HCl
相对分子质量:36.5
密度约1.18 g·mL-1
HCl的质量分数:36.5%
(1)该盐酸的物质的量浓度c(HCl)=__ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中(HCl)= ___mol·L-1。
(3)取稀释后盐酸溶液100mL,该溶液中所含的氯离子的个数为:N(Cl—)=___NA
(4)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液450 mL:
(1)配制溶液时,一般可以分为以下几个步骤:①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序为_________,本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有________。
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为___g,要完成本实验该同学应称出____g NaOH.。
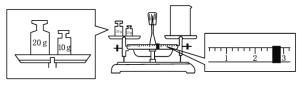
(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是____。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.FeCl3溶液中加入铜粉:2Fe3++3Cu=2Fe+3Cu2+
B.Al2O3溶于烧碱溶液:2Al3++3O2-+2OH-=2AlO![]() +H2O
+H2O
C.Al(OH)3溶于稀硫酸:Al(OH)3+3H+=Al3++3H2O
D.氢氧化钡溶液与硫酸溶液反应:Ba2++SO![]() =BaSO4↓
=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法中正确的是( )
A.标准状况下,11.2L CCl4中含有的分子数目为0.5 NA
B.1 mol Fe参与反应失去电子数目一定为2NA
C.1 molNa被完全氧化生成Na2O2,失去2NA个电子
D.常温下,46 g NO2和N2O4的混合物中含有的氮原子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com