
| A. | 3:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
分析 该反应中,铜失电子作还原剂,部分硝酸作氧化剂,根据反应方程式中元素化合价变化确定参加氧化还原反应的硝酸和未参加氧化还原反应的硝酸并结合N=nNA来解答.
解答 解:反应中N元素化合价降低,HNO3为氧化剂,Cu元素化合价升高,被氧化,根据方程式可判断,当8molHNO3参加反应时,有2mol被还原,表现为氧化性,6molHNO3表现为酸性,未被还原的HNO3与被还原的HNO3物质的量之比是3:1,根据N=nNA知未被还原的HNO3和被还原HNO3的分子个数比为3:1,
故选A.
点评 本题考查氧化还原反应的计算,把握反应中物质的量的关系为解答的关键,注意8mol硝酸反应时只有2mol作氧化剂被还原为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| B. | 金属钠可以通过电解熔融NaCl制得,推出金属铝可以通过电解熔融AlCl3制得 | |
| C. | 金属钠在纯氧中燃烧生成Na2O2,推出金属锂在纯氧中燃烧生成Li2O2 | |
| D. | CaCO3与稀硝酸反应生成CO2,推出CaSO3也能与稀硝酸反应生成SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑦ | B. | ③④⑦ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是物质的量的单位 | |
| B. | 国际上规定,0.012kg 12C原子所含有的碳原子数目的物质的量为1mol | |
| C. | mol H2的质量是2g,它所占的体积是 22.4L | |
| D. | 硫酸根离子的摩尔质量是 96g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
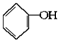 合成
合成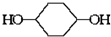 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).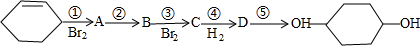
 、D
、D .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O
+2NaBr+2H2O .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用锌粒和稀硫酸制H2 | B. |  用H2O2和MnO2制O2 | ||
| C. | 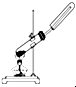 用氯化铵和氢氧化钙固体制NH3 | D. |  用铜片和稀硝酸制NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com