

 ;
; ;
; ;
; ;
;

 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
| A、2NH4Cl+Ca(0H)2═2NH3+2H20+CuCl2 |
| B、2Na202+2H20═4Na0H+02 |
| C、2S02+02═2S03 |
| D、Cu+2H2S04(浓)═CuS04+S02+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.
(R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.

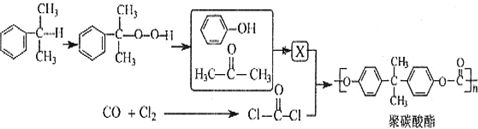
 反应合成聚碳酸酯的化学方程式(不必写反应条件):
反应合成聚碳酸酯的化学方程式(不必写反应条件): 互为同分异构体的有机物有
互为同分异构体的有机物有查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积等物质的量浓度的NaClO溶液与NaCl(aq) 溶液中离子总数大小:N后>N前 |
| B、常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
| C、0.1 mol?L-1Na2CO3溶液与0.1 mol?L-1NaHCO3溶液等体积混合c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
| D、硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
| OH- |
| H+ |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |

查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2min末,A和B的浓度之比为5:3 |
| B、x=1 |
| C、2min末,B的浓度为1.5 mol?L-l |
| D、2min末,A的消耗浓度为0.5 mol?L-l |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com