
【题目】以铝土矿为原料,提取氧化铝,冶炼铝的工艺流程如下,下列说法错误的是
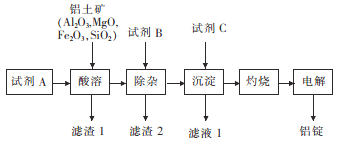
已知:滤渣2主要成分是氢氧化铁、氢氧化镁,B的焰色呈黄色。
A. 试剂A可以是稀硫酸或盐酸 B. 加入试剂B除去Mg2+、Fe3+
C. 滤渣1主要成分是SiO2 D. 电解氧化铝时在阴极上定期补炭块
科目:高中化学 来源: 题型:
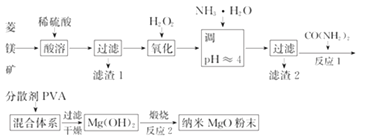
【题目】镁及其化合物有广泛用途.工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下
回答下列问题:
(1)滤渣1为____________(填化学式),CO(NH2)2的电子式为______。
(2)在实验室煅烧滤渣2制得的金属氧化物为______(填化学式),需要的仪器除酒精灯、三脚架以外,还需要______(填名称)。
(3)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,反应的化学方程式为__________。
(4)室温时,加入CO(NH2)2,产生沉淀。当 Mg2+沉淀完全时,溶液中的c(OH-)=_______(离子浓度小于1.0×10-5molL-1时,即可认为该离子沉淀完全;室温时,Ksp[Mg(OH)2]=1.96×10-11)
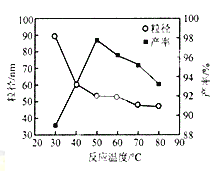
(5)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制务纳米MgO。如图为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届江苏省海安高级中学高三月考】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
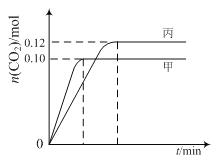
各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A.该反应的正反应为吸热反应
B.达到平衡时,乙中CO2的体积分数比甲中的小
C.T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)>v(逆)
D.T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行可逆反应,A跟B反应生成C,反应速率v(A)、v(B)、v(C)之间存在以下关系:v(B)=3v(A),v(c)=2v(A),3v(C)=2v(B)则该反应可以表示为( )
A. A+BC B. 2A+2B3C C. A+3B2C D. 3A+B2C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分元素的性质与原子(或分子)结构如下表所示:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的金属离子中半径最小 |
U | 第三周期元素的非金属离子还原性最弱 |
(1)写出元素T含有10个中子的原子符号:_________________。写出X与Y形成的化合物的电子式______________。
(2)Y与Z相比,金属性较强的是________(填元素符号),下列表能证明这一事实的是__________(填字母)。
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质与水反应剧烈
c.Y的化合价比Z低 d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)写出Z与U最高价氧化物对应的水合物相互反应的方程式____________________________
(4)M物质由T、Y、Z三种元素组成,请写出含0.1 mol的M溶液与60mL5 mol·L-1
的盐酸反应的离子反应式________________________________
(5)元素X与氢元素以原子个数比1∶2化合形成常用于火箭燃料的化合物元素T和氢元素以原子个数比为1∶1化合形成化合物Q,Q与W发生氧化还原反应,反应的产物不污染环境,写出该反应的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 凡是放热反应都是自发的,吸热反应都是非自发的
B. 自发反应的熵一定增大,非自发反应的熵一定减小或不变
C. ΔH<0、ΔS<0的反应一定能自发进行
D. ΔH>0、ΔS<0的反应一定不能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 铁粉溶于稀盐酸:2Fe+6H+=2Fe3++3H2↑
B. 碳酸钙溶于稀盐酸:CO32-+2H+=CO2↑+H2O
C. 氧化铜溶于醋酸:CuO+2CH3COOH =Cu2+ +2CH3COO- +H2O
D. 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-=BaSO4 ↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com