
把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水制成100 mL的混合溶液,用石墨作电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则下列描述正确的是
A.阳极得到的气体中有O2且为0.35 mol
B.铝元素仅以Al(OH)3的形式存在
C.阴极质量增加3.2 g
D.电路中共转移0.9 mol电子
D
【解析】
试题分析:根据离子的放电顺序,则在阴极放电的离子先是Cu2+, Cu2++2e-==Cu,其次是氢离子,发生2H++2e-==H2↑;在阳极放电的首先是氯离子,发生2Cl--2e-=Cl2↑,其次是氢氧根离子,发生2H2O -4e- =O2↑+4H+。根据题意,溶液中Cu2+的物质的量是0.1mol,氢离子的物质的量是0.2mol,氯离子的物质的量是0.5mol,一段时间后在两极收集到的气体在相同条件下体积相同,因为氢离子放电产生的氢气与氯离子放电产生的氯气的体积相等,所以阳极一定有氧气生成,所以阳极的氯离子一定放电完全。设阳极产生氧气的物质的量是x,则阳极:失去电子的物质的量是0.5mol+4x;则阴极产生氢气的物质的量是0.5mol/2+x,所以阴极:得到电子的物质的量是0.1mol×2+(0.5mol/2+x)×2,根据得失电子守恒,有0.5mol+4x=0.1mol×2+(0.5mol/2+x)×2,解得x=0.1mol。A、阳极得到的气体中有0.1mol氧气,错误;B、因为生成氢气的物质的量是0.35mol,则最终溶液呈碱性,硫酸根离子不放电,则铝元素以铝离子和氢氧化铝形式共同存在,错误;C、阴极增加的质量是0.1molCu的质量,为6.4g,错误;D、根据以上计算,电路中转移电子的物质的量是0.5mol+4x=0.9mol,正确,答案选D。
考点:考查电解原理的应用,离子放电顺序的判断,简单计算


科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:填空题
(12分)已知两种相邻周期、相邻主族的短周期非金属元素X、Y,其最高价氧化物的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
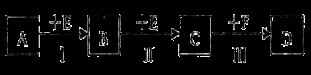
(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于____________(填“离子化合物”或“共价化合物”)。
②反应I的化学方程式为____________________________________________。
③将1.92g铜粉与一定量的D的浓溶液反应,当铜粉完全反应时收集到气体1.12L(标准状况),则反应消耗的D的物质的量为________________mol。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34 g/mol,则:
①将铜粉与D的浓溶液反应所得溶液加热蒸干,得到的白色固体物质为____________(填化学式)。
②将少景Na2Y溶液滴加到次氯酸钠溶液中发生反应,无沉淀生成,请写出该反应的离子反应方程式__________。在该反应中若有74.5 g NaClO被还原,则转移电子的物质的量为_________mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:选择题
利用图中所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合试卷(解析版) 题型:选择题
50℃时,0.1mol·L-1Na2CO3溶液pH=12,下列判断正确的是
A.c(OH-)=10-2mol·L-1
B.加入少量NaOH固体,c(Na+)和c(CO32-)均增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
D.2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:填空题
(10分)榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
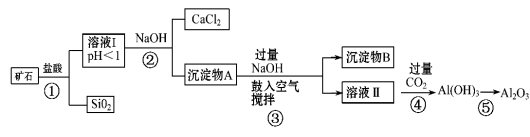
(1)SiO2的用途广泛,试写出其中的一种重要用途 ;
(2)溶液Ⅰ中除了Ca2+外,还含有的金属阳离子有 ;
(3)步骤③中NaOH参加反应的离子方程式是 ,
鼓入空气并充分搅拌的目的是(用化学方程式表示): 。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是 ________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
在一定条件下,RO3n-与R2-发生如下反应:RO3n-+2R2-+6H+=3R+3H2O下列关于元素R的叙述中正确的是
A.R原子的最外层上有4个电子 B.RO3n-中的R只能被还原
C.R的单质既有氧化性又有还原性 D.HnRO3一定是强酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度 | 溶解性 |
乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水和酒精以任意比互溶 |
A.萃取法 B.结晶法 C.分液法 D.蒸馏法
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省东莞市三校高二上学期期中联考化学试卷(解析版) 题型:选择题
在208 K、100 kPa时,已知:
2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
下列分子中含有手性碳原子的是
A.CF2Cl2
B.CH3CH2OH
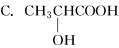
D.CH2===CH—COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com