
分析 将盛有18mLNO2的试管倒扣水中,NO2能和水发生反应:3NO2+H2O=2HNO3+NO,所剩余气体的体积的体积为原来气体体积的$\frac{1}{3}$,根据生成的硝酸的物质的量和所得溶液的体积来计算硝酸的浓度.
解答 解:将盛有22.4mLNO2的试管倒扣水中,n(NO2)=$\frac{0.0224L}{22.4L/mol}$=0.001mol,NO2能和水发生反应:3NO2+H2O=2HNO3+NO,
设生成的NO的体积为x,则有:
3NO2 +H2O=2HNO3 +NO
3 1
22.4mL x
3:1=22.4mL:x
x=$\frac{1×22.4mL}{3}$=7.47mL,
设生成硝酸的物质的量是y,
3NO2 +H2O=2HNO3 +NO
3 2
0.001mol y
y=$\frac{2×0.001}{3}$=0.0007mol,
进入溶液体积为消耗二氧化氮体积=22.4mL×$\frac{2}{3}$=15mL,
硝酸物质的量浓度=$\frac{\frac{2×0.001mol}{3}}{0.0224L×\frac{2}{3}}$=0.0446mol/L,
答:生成NO体积为7.47mL,生成硝酸物质的量浓度为0.0446mol/L.
点评 本题考查物质的量浓度的有关计算,侧重考查分析计算能力,利用方程式中各个物理量的关系进行计算,注意溶液体积不是二氧化氮气体体积,为易错点.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
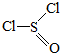 )主要用于制造酰基氯化物,其工业制备原理:
)主要用于制造酰基氯化物,其工业制备原理:| A. | SCl2和SOCl2中S的化合价分别为+2、+4价 | |
| B. | 制备反应中,二氧化硫是氧化产物 | |
| C. | 每消耗1mol SCl2,转移1mol电子 | |
| D. | SOCl2分子中既含有离子键又含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
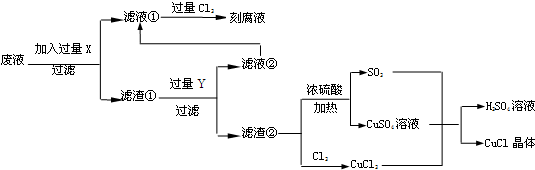
| 1 | 2 | 3 | |
| 0.25克样品消耗硫酸铈标准溶液的体积(mL) | 23.85 | 24.35 | 23.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的氢化物的水溶液呈酸性 | |
| B. | Y的氧化物和氢氧化物均不溶于水 | |
| C. | Z的最高价含氧酸的浓溶液有强氧化性 | |
| D. | W原子半径在同周期中最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com