
【题目】设NA代表阿伏加德罗常数,下列叙述正确的是( )
A. 1L CO的质量一定比1L O2的质量小
B. 将1 mol Cl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA
C. 常温常压下16 g O2和O3混合气体中,氧原子数为NA
D. 7.8 g Na2O2与足量水反应,转移电子数为0.2NA
【答案】C
【解析】A、气体的体积大小受温度和压强影响,标准状况下Vm=22.4L/mol;B、氯气与水反应是可逆反应;C、根据质量、原子数目与物质的量之间关系进行换算;D、1mol过氧化钠与水反应转移电子总数是NA。
气体的体积大小受温度和压强影响较大,A选项中没有指明温度和压强,气体的摩尔体积没有办法确定,即1L CO的物质的量和1L O2的物质的量大小没有办法确定,导致质量大小也没有办法确定,A选项错误;Cl2+H2O![]() HClO+HCl,该反应是可逆反应,N(HClO)+N(Cl-)+N(ClO-)=2NA成立的条件是所有氯气全部反应生成盐酸和次氯酸,所以B选项错误;16 g O2和O3混合气体中,氧原子的质量是16g,n(O)=16g/16g·mol-1=1mol,所以含有氧原子数为NA,C选项正确;从化学方程式2Na2O2+2H2O=4NaOH+O2↑可知,1mol过氧化钠完全反应转移电子总数是1mol,7.8g过氧化钠是0.1mol。转移电子总数是0.1mol,即0.1NA,D选项错误;正确选项C。
HClO+HCl,该反应是可逆反应,N(HClO)+N(Cl-)+N(ClO-)=2NA成立的条件是所有氯气全部反应生成盐酸和次氯酸,所以B选项错误;16 g O2和O3混合气体中,氧原子的质量是16g,n(O)=16g/16g·mol-1=1mol,所以含有氧原子数为NA,C选项正确;从化学方程式2Na2O2+2H2O=4NaOH+O2↑可知,1mol过氧化钠完全反应转移电子总数是1mol,7.8g过氧化钠是0.1mol。转移电子总数是0.1mol,即0.1NA,D选项错误;正确选项C。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】在酸性溶液中,能大量共存的离子组是( )
A. Al3+、Fe3+、Cl-、NO3- B. Mg2+、Ba2+、NO3-、SO42-
C. S2-、Na+、K+、Cl- D. Na+、 Fe3+ 、SO42-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表的相对位置如图所示,其中W元素原子的质子数是其最外层电子数的3倍,下列说法不正确的( )
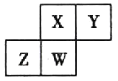
A. Z的单质常用于制造光导纤维
B. 简单氢化物的沸点:Y>X
C. X、Z、W的常见单质在一定条件下都可以与Y的常见单质反应
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴含量约为65mg·L-1,从海水中提取溴的工业流程如下:
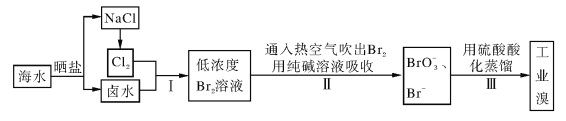
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是____。
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:_____
![]() Br2+
Br2+![]() CO32-===
CO32-===![]() BrO3-+
BrO3-+![]() Br-+
Br-+![]() CO2↑
CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是_____。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表达式错误的是
A. 甲烷的电子式:![]()
B. 碳原子的L层电子轨道表示式:![]()
C. 硫离子的核外电子排布式:1s22s22p63s23p6
D. 碳-12原子:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.
已知:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=﹣443.64kJmol﹣1
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1
下列说法或热化学方程式正确的是
A. CO的燃烧热为566.0 kJmol﹣1
B. 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低
C. 完全燃烧20g甲醇,生成二氧化碳和液态水时放出的热量为908.3 kJ
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H =﹣1453.28 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。关于该化合物的说法不正确的是( )
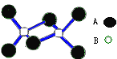
A. 化学式是Al2Cl6
B. 不存在离子键和非极性共价键
C. 在固态时所形成的晶体是分子晶体
D. 是离子化合物,在熔融状态下能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成S、C、Si三种元素的非金属性强弱比较的实验研究。乙同学设计了如图装置来验证卤族元素的性质递变规律,A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
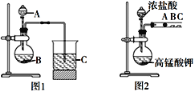
(1)如图中仪器A的名称是____。甲同学实验步骤:连接仪器、______、加药品、滴入试剂。
(2)①如图中仪器A中盛放试剂稀硫酸,烧瓶B中的盛放试剂为___溶液,C中的盛放试剂为______溶液。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是_________。
(3)如图中A处反应的离子方程式为__________。
(4)乙同学发现如图中B处试纸变蓝,C处红纸褪色,据此____(填“能”或“不能”)得出溴的非金属性强于碘,理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业以浓缩海水为原料提取溴的部分过程如下:
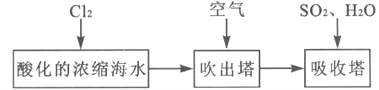
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
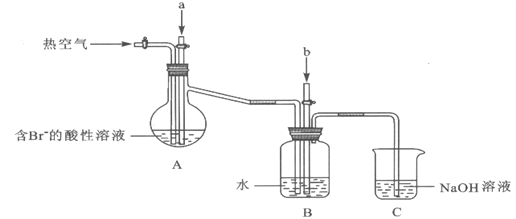
(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)_________。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是_________。
(3)反应过程中,B装置中Br2与SO2反应的化学方程式____________________。
(4)C装置的作用是___________________。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用____________________方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是________。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是:取出少量溶液,先加入过量新制氯水,再加入KI淀粉溶液,观察溶液是否变蓝色。该方案是否合理并简述理由: _______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com