
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液的体积/ml | 25.52 | 25.02 | 24.98 |
分析 (1)根据二价铁易发生水解反应分析;FeSO4溶液变质后生成Fe3+;
(2)步骤3是由溶液中获得晶体,是抑制亚铁离子的水解下的蒸发与结晶过程;
(3)依据该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇分析,洗涤不能溶解产品,不能引入新的杂质;
(4)称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定,
①发生的反应为高锰酸钾溶液氧化亚铁离子为铁离子;
②反应终点的判断可以利用高锰酸钾溶液的紫红色判断,滴入最后一滴溶液变化为紫红色,半分钟内不变,证明反应达到终点;
③依据反应的定量关系计算亚铁离子物质的量,得到(NH4)2SO4•FeSO4•6H2O的质量,计算纯度,高锰酸钾溶液的体积第一次误差较大,应舍去;
④a.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积,液面被提高,读取体积减小;
b.滴定前滴定管尖嘴有气泡,滴定结束无气泡测定溶液体积增大;
c.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,待装液润洗会增多消耗高锰酸钾溶液的体积,测定结果增大;
d.该酸性高锰酸钾标准液未用硫酸酸化,改用硝酸酸化,消耗的高锰酸钾体积减少.
解答 解:(1)由于FeSO4易发生水解,故加入稀硫酸来抑制其水解;FeSO4溶液变质后生成Fe3+,故取适量FeSO4溶液于试管中,向溶液中加入KSCN溶液,若溶液变红,则说明FeSO4溶液变质,
故答案为:抑制FeSO4的水解;取适量FeSO4溶液于试管中,向溶液中加入KSCN溶液,若溶液变红,则说明FeSO4溶液变质,无现象则不变质;
(2)步骤3是由溶液中获得晶体,亚铁离子在加热过程中会发生水解,应在抑制亚铁离子的水解情况下,蒸发浓缩、冷却结晶、过滤、洗涤等.
故答案为:蒸发浓缩;冷却结晶;
(3)因为硫酸亚铁铵易溶于水,不溶于乙醇,应该用乙醇洗涤,减少硫酸亚铁铵的溶解,同时利用乙醇和水互溶,从而达到洗涤的要求,故选d,
故答案为:d;
(4)①利用高锰酸钾的强氧化性,Fe2+的强还原性,两者发生氧化还原反应,Fe2+被氧化成Fe3+↑1,Mn由+7价→+2↓5,最小公倍数5,根据原子个数、电荷守恒,即MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
②向溶液中滴加中高锰酸钾,高锰酸钾显紫红色,因此滴定到终点:最后一滴滴入,溶液由无色变为浅紫色,且30s不变色,
故答案为:最后一滴滴入,溶液由无色变为浅紫色,且30s不变色;
③因为第一次与第二次、第三次相差较大,忽略不计,消耗高锰酸钾溶液的体积为$\frac{25.02+24.98}{2}$ml=25mL,根据离子反应方程式,得出:n[(NH4)2SO4•FeSO4•6H2O]=5n(KMnO4)=25×10-3×c×5mol,则500mL溶液中含有n[(NH4)2SO4•FeSO4•6H2O]=25×10-3×c×5×500/25mol=2.5cmol,
所以质量分数=2.5c×$\frac{392}{a}$×100%=$\frac{980c}{a}$×100%,
故答案为:$\frac{980c}{a}$×100%;
a、俯视读数,造成所读的数偏小,故a错误;
b、滴定管尖嘴有气泡,滴定结束无气泡,所消耗的液体体积增加,故b正确;
c、锥形瓶用待测液润洗,待测液的物质的量增加,则消耗高锰酸钾的体积增加,故c正确;
d、该酸性高锰酸钾标准液未用硫酸酸化,改用硝酸酸化,硝酸具有氧化性,也会也会亚铁离子,消耗的高锰酸钾体积减少,故d错误.
故答案为:bc.
点评 本题考查了液的加热、过滤、固体溶解、蒸发(防水解)、结晶等一系列实验基本操作、离子检验等氢氧化亚铁制备的非常规制备方法和实验过程分析判断,滴定实验的注意问题和计算应用,注意掌握物质性质,实验过程的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
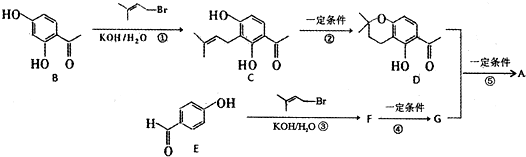
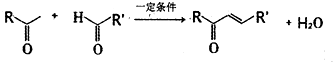
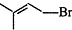 生成高分子化合物的方程式
生成高分子化合物的方程式 .
. 、
、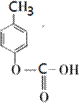 .
.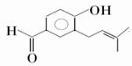 .
.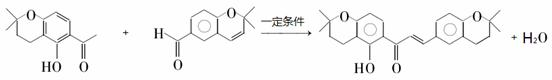 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
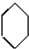 $→_{①}^{Cl_{2},光照}$
$→_{①}^{Cl_{2},光照}$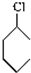 $→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$
$→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$ $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$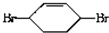 $\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$
$\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$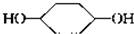
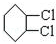 ,C
,C
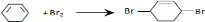 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与P4的分子结构都是正四面体形,因此在6.02×1023个CH4分子或P4分子中都含有4×6.02×1023个共价键 | |
| B. | 在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键 | |
| C. | 28g CO、C2H4混合气体的分子总数NA,体积约为22.4L | |
| D. | 6.02×1023个Fe3+完全水解可以得到6.02×1023个氢氧化铁胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 石油的蒸馏实验中,加入碎瓷片可防止石油在蒸馏时暴沸 | |
| B. | 乙醇的催化氧化实验中铜丝主要起氧化剂的作用 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入乙酸,最后加入浓硫酸 | |
| D. | 在淀粉溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明淀粉没有水解 | |
| E. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性溶KMnO4液 | |
| F. | 用钠可以检验某无水酒精中是否含有水 | |
| G. | 可用溴水来鉴别植物油和矿物油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
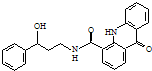
| A. | X的分子式为C23H25N2O3 | |
| B. | 每个X分子中含有2个肽键 | |
| C. | 1molX最多能与9molH2发生加成反应 | |
| D. | X能发生水解、氧化和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2与18O2互为同素异形体 | |
| B. | Na2S的电子式为: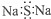 | |
| C. | 熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO42- | |
| D. | 钢铁表面常常出现的铁锈的主要成分是Fe2O3•xH2O,它不能阻止钢铁继续腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
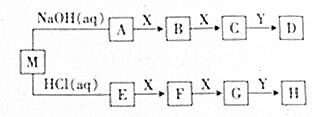 几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.
几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.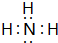 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
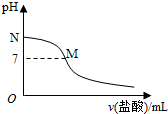
| A. | 该滴定过程应该选择酚酞作为指示剂 | |
| B. | M点对应的盐酸体积为20.0mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com