
某实验小组用下列装置进行乙醇催化氧化的实验。
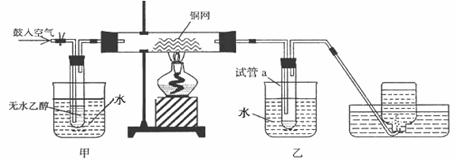
(1)、实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,
说明该乙醇催化反应是_____ 反应。
(2)、甲和乙两个水浴作用不相同。
甲的作用是____________; 乙的作用是_______________。
(3)、反应进行一段时间后,干燥试管a中能收集到不同的物质,
它们是 __。
集气瓶中收集到的气体的主要成分是____________ 。
(4)、试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________________ 。
要除去该物质,可在混合液中加入_____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过___________________(填实验操作名称)即可除去。
科目:高中化学 来源: 题型:
下列实验中操作、现象、结论对应关系正确的一组是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 | 只体现了浓硫酸的脱水性 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液 | 生成淡黄色沉淀 | 溴乙烷中含有溴元素 |
| D | 将溴水加入苯中并充分振荡 | 溴水褪色 | 苯与溴发生了取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是 ( )。

查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制氯气有如下几步操作:①在烧瓶内装入MnO2粉末;②塞好带导管和分液漏斗的双孔塞;③由分液漏斗向烧瓶中注入浓盐酸;④用铁夹固定圆底烧瓶;⑤检查气密性;⑥放好酒精灯;⑦点燃酒精灯;⑧放好铁圈和石棉网,正确的操作顺序是
A.①②③④⑧⑤⑥⑦ B.⑤①②③⑧④⑥⑦
C.⑤⑥⑧①②③④⑦ D.⑥⑧⑤①②④③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室进行物质制备,下列从原料及有关试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合 理的是
理的是
A.C CO
CO CO2
CO2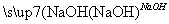 Na2CO3
Na2CO3
B.Cu Cu(NO3)2溶液
Cu(NO3)2溶液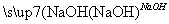 Cu(OH)2
Cu(OH)2
C.CaO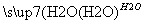 Ca(OH)2溶液
Ca(OH)2溶液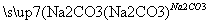 NaOH溶液
NaOH溶液
D.Fe Fe2O3
Fe2O3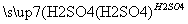 Fe2(SO4)3溶液
Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,AgBr的Ksp=4.9×10-13、AgI的Ksp=8.3×10-17。
(1)现向含有AgI的饱和溶液中:
①加入固体AgNO3,则c(I-)________(填“变大”、“变小”或“不变”,下同);
②若改加更多的AgI,则c(Ag+)________;
③若改加AgBr固体,则c(I-)____________________;而c(Ag+)________。
(2)有关难溶盐的溶度积及溶解度(与AgBr、AgI无关),有以下叙述,其中正确的是________。
A.两种难溶盐电解质,其中Ksp小的溶解度一定小
B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变
C.将难溶 电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积
电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积
D.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀
E.难溶盐电解质的Ksp和温度有关
F.加入与原难溶电解质具有相同离子的物质,使难溶电解质的溶解度变小,也使Ksp变小
(3)现向含有NaBr、KI均为0.002 mol/L的溶液中加入等体积的浓度为4×10-3 mol/L AgNO3溶液,则产生的沉淀是________(填化学式);若向其中再加入适量的NaI固体,则最终可发生沉淀转化的总反应式表示为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________,该能层具有的原子轨道数为______。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H22NH3实现储氢和输氢。下列说法正确的是________________________________________________________________________。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH 与PH
与PH 、CH4、BH
、CH4、BH 、ClO
、ClO 互为等电子体
互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+中N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是________________________________________________________________________
________________________________________________________________________。
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图G133所示:

图G133
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的Cl-的个数为______,该Na+与跟它次近邻的Cl-之间的距离为______。
(2)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为________________________________________________________________________
(用含a、b的式子表示)。
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com