
【题目】下列说法正确的是 ( )
A.所有化学反应都能设计成原电池
B.原电池工作时,溶液中阳离子向负极移动,盐桥中阳离子向正极移动
C.在原电池中,负极材料活泼性一定比正极材料强
D.原电池放电时,电流方向由正极沿导线流向负极
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3===7N2+12H2O构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是()

A. 电流从左侧电极经过负载后流向右侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为2NH3-6e-===N2+6H+
D. 当有4.48 L NO2被处理时,转移电子数为0.8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能源、能量转化及其说法正确的是( )
A.化石能源是可再生能源
B.太阳能不是清洁能源
C.能量在转化或转移的过程中总量保持不变
D.核能只能通过重核裂变获取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛是生产金属钛及其化合物的重要中间体。某校化学课外活动小组准备利用下图装置制备四氯化钛(部分夹持仪器已略去)。
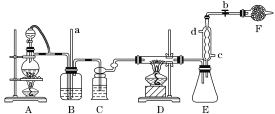
资料表明:室温下,四氯化钛为无色液体,熔点:-25 ℃,沸点:136.4 ℃。在空气中发烟生成二氧化钛固体。在650~850 ℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。回答下列问题:
(1)实验时在仪器中加试剂前要先___________________________。
(2)实验中分液漏斗上口玻璃塞连接导管的作用是__________________________________ B装置的作用是_____________________________。
(3)写出D装置中物质制备的化学方程式________________________________;写出四氯化钛在空气中发烟的化学方程式______________________________。
(4)E装置作用是_______________________。
(5)F装置中盛装的物质是________。
(6)该实验设计略有缺陷,请指出其不足之处:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,盐酸与氢氧化钠溶液相互滴定的滴定曲线如下图,下列叙述不正确的是
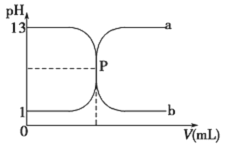
A. 滴定过程的任何时刻都存在:c(H+)+ c(Na+)=c(OH-)+c(Cl-)
B. 曲线b是用氢氧化钠溶液滴定盐酸溶液的滴定曲线
C. 氢氧化钠溶液的物质的量浓度为0.1molL-1
D. P点时恰好完全中和,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,参照元素①~⑨在表中的位置,按要求回答下列问题:
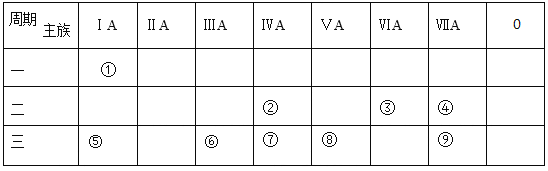
(1)在元素①~⑨,最活泼的金属元素是______(填元素名称);最活泼的非金属元素名称是______(填元素名称)
(2)用电子式表示元素③与⑤形成的原子个数比为1∶2的化合物 ______。元素①和③所形成的化学键的类型是_______。
(3)②、⑤、⑦三种元素的原子半径由大到小的顺序是______(用元素符号表示)。
(4)元素④和⑨所能形成的气态氢化物的稳定性______(用化学式表示);元素⑦、⑧、⑨的最高价氧化物对应的水化物的酸性由强到弱的顺序______(用化学式表示);
(5)写出元素![]() 和
和![]() 的最高价氧化物的水化物相互反应的离子方程式:______。
的最高价氧化物的水化物相互反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 灼热的炭与CO2反应 B. 氧化铁与铝反应
C. 钠与乙醇反应 D. Ba(OH)2·8H2O与NH4C1反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲是一种利用微生物将废水中的尿素(CO(NH2)2)的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )
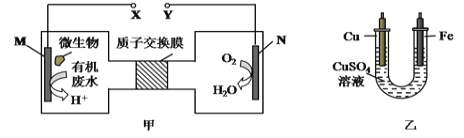
A. 铜电极应与X相连接
B. H+透过质子交换膜由右向左移动
C. 当N电极消耗0.25mol气体时,则铁电极增重16g
D. M电极反应式:H2NCONH2+H2O-6e-==CO2↑+N2↑+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列说法正确的是
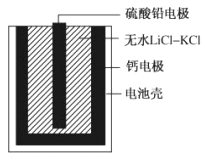
A. 放电过程中,Li+向负极移动
B. 正极反应式:Ca+2Cl-—2e-=CaCl2
C. 每转移0.1mol电子,理论上生成10.35gPb
D. 常温时,在正负极间接上电流表或检流计,指针偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com