
 ����ͼ��ʾװ�ý�������ˮ�ķ�Ӧʵ�飬��ش��������⣺
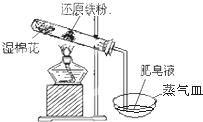
����ͼ��ʾװ�ý�������ˮ�ķ�Ӧʵ�飬��ش��������⣺���� ��1��ʵ��ǰ���������װ�ý��������Լ�飻
��2������ˮ������Ӧ����Fe3O4��H2��
��3������ˮ����������������ȼ�����������ڵ�ȼʱ���б�������
��4��ʵ�����ʱ��Ҫ��ֹҺ�嵹����
��5��װ����ȴ���ԹܵIJ�������Ϊ������������������Fe��
��� �⣺��1��װ�ð�װ���ʵ��ǰ���������װ�ý��������Լ�飬�ʴ�Ϊ�����װ�õ������ԣ�
��2������ˮ��������������ԭ��Ӧ������Fe3O4��H2����Ӧ����ʽΪ��3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
�ʴ�Ϊ��3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
��3������ˮ����������������Ӧһ��ʱ����з����ݴ���ʱ���õ�ȼ�Ļ�������ݣ������ݱ�ը�������������ڵ�ȼʱ���б�������
�ʴ�Ϊ�������ݱ�ը����������������
��4��ʵ�����ʱ��Ϊ�˷�ֹ�������е�Һ���ڴ���ѹ�������£�˳�ŵ��ܵ������Թ��У�Ӧ���ȳ������ܣ������߾ƾ��ƣ�
�ʴ�Ϊ���ȳ������ܣ������߾ƾ��ƣ���ֹҺ�嵹����
��5������ˮ��������������ԭ��Ӧ������Fe3O4��H2��װ����ȴ���ԹܵIJ���������ҪΪFe3O4����������û�з�Ӧ��ȫ�������ʣ����߾�Ϊ��ɫ���壬
�ʴ�Ϊ���ڣ�
���� �����ǹ��ڽ�������ˮ��Ӧ��ʵ�鷽����ƺ����ۣ�����Ĺؼ������շ�Ӧ��������ʣ����ʼ����Լ�ʵ�������ȫ�Ȼ���֪ʶ���ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��b �Ľṹ��ʽ
��b �Ľṹ��ʽ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
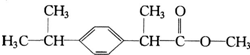 �����л���X��˵���У�������ǣ�������
�����л���X��˵���У�������ǣ�������| A�� | X������ˮ���������л��ܼ� | B�� | 1molX�ܸ�4 mol���������ӳɷ�Ӧ | ||
| C�� | X��ʹ���Ը��������Һ��ɫ | D�� | X��ˮ����ﲻ�ܷ�����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol•L-1 HA ��c��H+��=c��OH-��+c��A-���� | |
| B�� | 0.1mol•L-1 HA �� 0.1 mol•L-1NaOH �������Һ�����ԣ�c��Na+����c��A-�� | |
| C�� | 0.1mol•L-1 NaA ��c��Na+����c��OH-����c��A-����c��H+�� | |
| D�� | 0.1mol•L-1 HA�м�������NaA���壬HA�ĵ��볣����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | Ԥ������ͽ��� | |
| ����1 | ������������Һ������A��B�Թ��У� | |
| ����2 | ||
| ����3 | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ı��¶ȣ���Ӧ��ת�Ƶ��ӵ����ʵ���n�ķ�Χ��3amol��n��5amol | |
| B�� | �ı��¶ȣ�������NaCl����С���۲���Ϊ4amol | |
| C�� | �μӷ�Ӧ�����������ʵ���3amol | |
| D�� | ij�¶��£�����Ӧ��$\frac{c��C{l}^{-}��}{c��Cl{O}^{-}��}$=6������Һ��$\frac{c��C{l}^{-}��}{c��C{O}_{3}^{-}��}=\frac{1}{2}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʱ����ζ����ѧ�仯�� | |
| B�� | ���������ѣ���ѧ�仯�� | |
| C�� | ������̼ʹ�����ʯ��ˮ����ǣ������仯�� | |
| D�� | ��������Ⱥ��Ϊ���������仯�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com