
下列说法中正确的是(NA表示阿伏加德罗常数)()
A. 常温常压下,22.0 gCO2所含的电子数为22NA
B. 常温常压下,1mol氦气含有原子数为NA
C. 0.5mol•L﹣1 Na2CO3溶液中含有Na+离子的数目为NA
D. 标准状况下,22.4LCCl4含有的氯原子数为4NA
考点: 阿伏加德罗常数.
分析: A、根据二氧化碳的物质的量和1molCO2含22mol电子;
B、氦气是单原子分子;
C、溶液体积不明确;
D、标况下,四氯化碳为液态.
解答: 解:A、22g二氧化碳的物质的量为0.5mol,而1molCO2含22mol电子,故0.5molCO2含11mol电子,个数为11NA个,故A错误;
B、氦气是单原子分子,故1mol氦气含有原子数为NA,故B正确;
C、溶液体积不明确,无法计算Na+离子的数目,故C错误;
D、标况下,四氯化碳为液态,故D错误.
故选B.
点评: 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
某短周期元素R,它的最高价氧化物中含氧为60%,它的氢化物中含R为94.12%.R元素原子核内质子数和中子数相等.通过计算求R元素的相对原子质量,并指出它在周期表中的位置.(已知氧元素的相对原子质量为16)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是()
A. Y的阴离子Y﹣的还原性强于X的阴离子X﹣
B. X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强
C. X的单质X2能将Y的阴离子Y﹣氧化成Y2
D. X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和.
(1)写出A的原子结构示意图 .
(2)D的质子数和中子数相等,D的原子组成符号为 .
(3)用电子式表示A、D两元素形成AD2的过程: ;写出C2B2的电子式 .
(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是 .
(5)写出甲和A的最高价氧化物反应的化学方式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中数据合理的是()
A. 用10 mL 量筒量取5.2 mL盐酸
B. 用广泛pH试纸测得某溶液的pH值为12.5
C. 用托盘天平称取25.12gNaCl固体
D. 用100 mL容量瓶配制50mL0.1 mol/L的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,既属于化合反应,又属于氧化还原反应的是()
A. H2+Cl2 2HCl B. 2H2O2
2HCl B. 2H2O2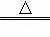 2H2O+O2↑
2H2O+O2↑
C. CaO+H2O=Ca(OH)2 D. Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com