
【题目】工业上用铁矿石、焦炭、空气、石灰石为原料来冶炼铁。
(1)请写出用磁铁矿在高温下冶炼铁的化学方程式___________。请你用化学方法设计实验方案检验上述反应得到的固体产物中含有铁粉___________。
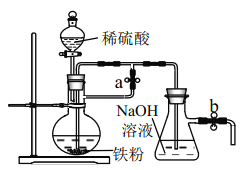
(2)小明同学将用冶炼所得的铁粉按下图装置来制备 Fe(OH)2,实验开始时应先_______活塞a,___________活塞 b(填“打开”或“关闭”)
【答案】 Fe3O4 +4CO![]() 3Fe+4CO2 方法 1:在黑色粉末中加入稀硫酸(稀盐酸),如果有气泡生成,则是铁粉;方法 2:在黑色粉末中加入硫酸铜溶液,如果黑色粉末表面有红色固体析出,则是铁粉 打开 打开
3Fe+4CO2 方法 1:在黑色粉末中加入稀硫酸(稀盐酸),如果有气泡生成,则是铁粉;方法 2:在黑色粉末中加入硫酸铜溶液,如果黑色粉末表面有红色固体析出,则是铁粉 打开 打开
【解析】(1)磁铁矿主要成分为Fe3O4,过量的碳与氧气高温下反应生成CO,Fe3O4被CO还原为Fe,化学方程式Fe3O4 +4CO![]() 3Fe+4CO2;正确答案:Fe3O4 +4CO
3Fe+4CO2;正确答案:Fe3O4 +4CO![]() 3Fe+4CO2 。反应后的生成物中一定含有铁粉,利用金属铁和稀硫酸反应放氢气或铁从硫酸铜溶液中置换出铜的性质就可以检验出生成物中是否含有金属铁;正确答案:方法 1:在黑色粉末中加入稀硫酸(稀盐酸),如果有气泡生成,则是铁粉;方法 2:在黑色粉末中加入硫酸铜溶液,如果黑色粉末表面有红色固体析出,则是铁粉 。
3Fe+4CO2 。反应后的生成物中一定含有铁粉,利用金属铁和稀硫酸反应放氢气或铁从硫酸铜溶液中置换出铜的性质就可以检验出生成物中是否含有金属铁;正确答案:方法 1:在黑色粉末中加入稀硫酸(稀盐酸),如果有气泡生成,则是铁粉;方法 2:在黑色粉末中加入硫酸铜溶液,如果黑色粉末表面有红色固体析出,则是铁粉 。
(2)Fe(OH)2还原性很强,易被空气中氧气氧化变为Fe(OH)3,因此在制备Fe(OH)2沉淀时,一定要避免空气的干扰;实验开始时应先排净装置内的空气,因此先打开活塞a和活塞b,利用铁和硫酸反应产生的氢气来实现此目的;然后关闭活塞a,就可以在锥形瓶中看到白色沉淀;正确答案: 打开; 打开。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
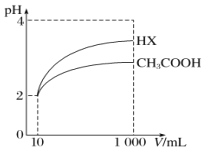
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“小于”或“等于”)醋酸的电离平衡常数,理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,用 Fe2O3、 NiO 或 Cr2O3作催化剂对燃煤烟气进行回收,使 SO2转化生成为 S。催化剂不同,相同其他条件(浓度、温度、压强)情况下, 相同时间内 SO2 的转化率随反应温度的变化如下图:下列说法不正确的是( )
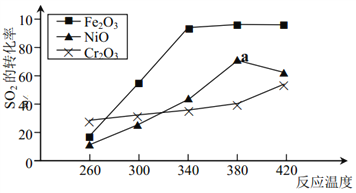
A. 不考虑催化剂价格因素,选择 Fe2O3 作催化剂可以节约能源
B. 相同其他条件下,选择 Cr2O3 作催化剂, SO2 的平衡转化率最小
C. a 点后 SO2 的转化率减小的原因可能是温度升高催化剂活性降低了
D. 选择 Fe2O3 作催化剂,最适宜温度为 340~380℃温度范围
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)乙炔是一种重要的化工原料,最新研制出的由裂解气(H2、CH4、C2H4)与煤粉在催化剂条件下制乙炔,该生产过程是目前清洁高效的煤化工过程。已知:发生的部分反应如下(在25℃、 101 kPa时),CH4、C2H4 在高温条件还会分解生成炭与氢气:
①C (s) +2H2(g)![]() CH4(g) △H1=-74.85kJmol-1
CH4(g) △H1=-74.85kJmol-1
②2CH4(g)![]() C2H4(g) +2H2(g) △H2=340.93kJmol-1
C2H4(g) +2H2(g) △H2=340.93kJmol-1
③C2H4(g)![]() C2H2(g) +H2(g) △H3=35.50kJmol-1
C2H2(g) +H2(g) △H3=35.50kJmol-1
请回答:
(1)依据上述反应, 请写出 C 与 H2化合生成 C2H2 的热化学方程式:______________。
(2)若以乙烯和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有乙烯、乙炔、氢气等。图1 为乙炔产率与进料气中 n(氢气)/n(乙烯)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是______________。
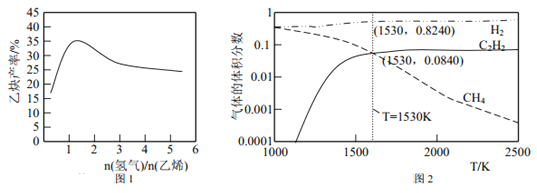
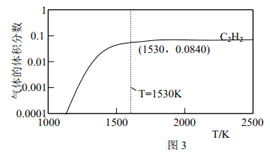
(3)图 2 为上述诸反应达到平衡时各气体体积分数和反应温度的关系曲线。
①乙炔体积分数在1530℃之前随温度升高而增大的原因可能是_______________;1530℃之后,乙炔体积分数增加不明显的主要原因可能是_______________。
②在体积为1L的密闭容器中反应,1530℃时测得气体的总物质的量为1.000 mol,则反应C2H4(g)![]() C2H2(g) +H2(g) 的平衡常数 K=_______________。
C2H2(g) +H2(g) 的平衡常数 K=_______________。
③请在图3中绘制乙烯的体积分数和反应温度的关系曲线__________。
(二)当今,人们正在研究有机锂电解质体系的锂-空气电池,它是一种环境友好的蓄电池。放电时电池的总反应为:4Li+O2===2Li2O。在充电时,阳极区发生的过程比较复杂,目前普遍认可的是按两步进行,请补充完整。电极反应式: ________________________和 Li2O2-2e-=2Li++O2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与N2O4可相互转化:2NO2(g)![]() N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )
N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )

A. 前10 min内,用v(NO2)表示的反应速率为0.04 mol·L-1·min-1
B. 反应进行到10 min时,体系放出的热量为9.68 kJ
C. a点正反应速率小于逆反应速率
D. 25 min时,正反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸(HNO2)为一元弱酸,其性质与硝酸相似。已知:298K时,四种物质的电离平衡常数(K)如下表。
HNO2 | NH3·H2O | H2CO3 | H2SO3 | |
K(mol·L-1)-2 | 5.1×10-4 | 1.8×10-5 | Ka1=4.2×10-7 Ka2=5.61×10-11 | Ka1=1.3×10﹣2 Ka2=6.3×10﹣8 |
(1)下列不能说明HNO2是弱电解质的是_____。
A.常温下0.1 mol·L-1 NaNO2溶液的pH>7
B.用一定浓度HNO2溶液做导电实验,灯泡很暗
C.等pH、等体积的盐酸和HNO2溶液分别与足量锌反应,HNO2放出的氢气较多
D.常温下,0.1mol·L-1 HNO2溶液的pH=2.3
(2)298K时,将10mL 0.1mol·L-1的亚硝酸溶液与10mL 0.1mol·L-1氨水混合,所得溶液为_____(填“酸性”、“碱性”或“中性”),原因是___________________________。
(3)若将pH=2的HNO2、HCl两溶液分别加水稀释,pH变化如右图所示,判断曲线I对应的溶液为_______(填化学式)。图中a、b、c三点对应溶液的导电能力由强到弱的顺序是
________(用a、b、c表示,下同);溶液中水的电离程度由强到弱的顺序是________。

(4)依据提供数据回答下列问题。
①求298K时,NaHSO3溶液中HSO3-水解平衡常数Kh =____;由此可判断HSO3-水解程度______电离程度(填“>”、“<”或“=”)。
②H 2SO3溶液和NaHCO3溶液反应的主要离子方程式为______。
(5)298K时,向含有2mol Na2CO3的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为短周期主族元素,已知它们的原子序数的关系为X+Z=2Y,且Z的最高价氧化物对应的水化物是强酸。则下列有关说法正确的是
A. 若X是Na,则Z的最高价一定为偶数
B. 若X是O,则YX一定是离子化合物
C. 若Y是O,则非金属性Z>Y>X
D. 若Y是Na,则X、Z不可能是同一主族元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com