
| A£® | µ„Ī»Ź±¼äÄŚÉś³Én molµÄA2£¬Ķ¬Ź±Éś³Én molµÄAB | |
| B£® | ČŻĘ÷ÄŚµÄ×ÜŃ¹Ēæ²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»Æ | |
| C£® | µ„Ī»Ź±¼äÄŚÉś³É2n molµÄABĶ¬Ź±Éś³Én molµÄB2 | |
| D£® | Ę½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»Ėꏱ¼ä±ä»Æ¶ų±ä»Æ |
·ÖĪö øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷½ā“š£¬µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷ĪļÖŹµÄÅØ¶Č”¢°Ł·Öŗ¬Įæ²»±ä£¬ŅŌ¼°ÓÉ“ĖŃÜÉśµÄŅ»Š©ĮæŅ²²»·¢Éś±ä»Æ£¬½āĢāŹ±ŅŖ×¢Ņā£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£®
½ā“š ½ā£ŗA”¢ĖŁĀŹÖ®±Č²»µČÓŚ¶ŌÓ¦ĪļÖŹµÄ»Æѧ¼ĘĮæŹżÖ®±Č£¬¹ŹA“ķĪó£»
B”¢Į½±ßµÄĘųĢå¼ĘĮæŹżĻąµČ£¬ČŻĘ÷ÄŚŃ¹ĒæŹ¼ÖÕ±£³Ö²»±ä£¬²»ÄÜĖµĆ÷“ļĘ½ŗāדĢ¬£¬¹ŹB“ķĪó£»
C”¢µ„Ī»Ź±¼äÄŚÉś³É2n molµÄABµČŠ§ÓŚĻūŗÄn molµÄB2Ķ¬Ź±Éś³Én molµÄB2£¬ĖµĆ÷“ļĘ½ŗāדĢ¬£¬¹ŹCÕżČ·£»
D”¢øł¾ŻÖŹĮæŹŲŗć£¬×ÜÖŹĮæŹ¼ÖÕ²»±ä£¬×ÜĪļÖŹµÄĮæŹ¼ÖÕĻąµČ£¬ĖłŅŌĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæŹ¼ÖÕ²»Ėꏱ¼ä±ä»Æ¶ų±ä»Æ£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ£¬ÄŃ¶Č²»“ó£¬×¢Ņāµ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬µ«²»ĪŖ0£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | a+b£¼c+d£¬Q£¾0 | B£® | a+b£¾c+d£¬Q£¾0 | C£® | a+b£¼c+d£¬Q£¼0 | D£® | a+b=c+d£¬Q£¾0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Al2£ØSO4£©3 ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++3OH-=Al£ØOH£©3”ż | |
| B£® | µē½ā±„ŗĶŹ³ŃĪĖ®£ŗ2Cl-+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$H2”ü+Cl2”ü+2OH- | |
| C£® | Ģ¼ĖįøĘÓėŃĪĖį·“Ó¦£ŗCaCO3+2H+=Ca2++CO2”ü+H2O | |
| D£® | FeSO4 ČÜŅŗÖŠ¼ÓČėÓĆĮņĖįĖį»ÆµÄH2O2ČÜŅŗ£ŗFe2++H2O2+2H+=Fe3++2 H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
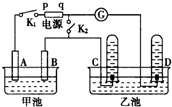 ŌŚĶ¼¾łÓĆŹÆÄ«×÷µē¼«µÄµē½ā³ŲÖŠ£¬¼×³ŲÖŠĪŖ500mLŗ¬Ä³Ņ»ČÜÖŹµÄĄ¶É«ČÜŅŗ£¬ŅŅ³ŲÖŠĪŖ500mLĻ”ĮņĖį£¬±ÕŗĻK1£¬¶ĻæŖK2½ųŠŠµē½ā£¬¹Ū²ģµ½Aµē¼«±ķĆęÓŠŗģÉ«µÄ¹ĢĢ¬ĪļÖŹÉś³É£¬Bµē¼«ÓŠĪŽÉ«ĘųĢåÉś³É£»µ±ČÜŅŗÖŠµÄŌÓŠČÜÖŹĶźČ«µē½āŗó£¬Ķ£Ö¹µē½ā£¬Č”³öAµē¼«£¬Ļ“µÓ”¢øÉŌļ”¢³ĘĮ棬µē¼«ŌöÖŲ1.6g£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŌŚĶ¼¾łÓĆŹÆÄ«×÷µē¼«µÄµē½ā³ŲÖŠ£¬¼×³ŲÖŠĪŖ500mLŗ¬Ä³Ņ»ČÜÖŹµÄĄ¶É«ČÜŅŗ£¬ŅŅ³ŲÖŠĪŖ500mLĻ”ĮņĖį£¬±ÕŗĻK1£¬¶ĻæŖK2½ųŠŠµē½ā£¬¹Ū²ģµ½Aµē¼«±ķĆęÓŠŗģÉ«µÄ¹ĢĢ¬ĪļÖŹÉś³É£¬Bµē¼«ÓŠĪŽÉ«ĘųĢåÉś³É£»µ±ČÜŅŗÖŠµÄŌÓŠČÜÖŹĶźČ«µē½āŗó£¬Ķ£Ö¹µē½ā£¬Č”³öAµē¼«£¬Ļ“µÓ”¢øÉŌļ”¢³ĘĮ棬µē¼«ŌöÖŲ1.6g£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | µē½āŹ±£¬ŹÆÄ«×÷Ņõ¼«£¬Ģś×÷Ńō¼« | |
| B£® | Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2H++2e-ØTH2”ü | |
| C£® | µē½ā¹ż³ĢÖŠŃō¼«ÖÜĪ§ČÜŅŗµÄpH±ä“ó | |
| D£® | ĄķĀŪÉĻĆæÉś³É1molKIO3ŌņµēĀ·ÖŠĮ÷¹ż6mole- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ė²¼ä²śÉś“óĮæøßĪĀĘųĢåĶʶÆŗ½Ģģ·É»ś·ÉŠŠ | |
| B£® | “ÓÄÜĮæ±ä»ÆµÄ½Ē¶Č£¬Ö÷ŅŖŹĒ»ÆѧÄÜ×Ŗ±äĪŖČČÄÜŗĶ¶ÆÄÜ | |
| C£® | ·“Ó¦µÄģŹ±ä“óÓŚĮć | |
| D£® | ŌŚ·½³ĢŹ½ŗóŌö¼Ó”÷H¼°Ę䏿ֵ¼“ĪŖČČ»Æѧ·½³ĢŹ½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŪČŚµÄKCl | B£® | NaClČÜŅŗ | C£® | ŅŗĢ¬ĀČ»ÆĒā | D£® | NaCl¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįÄʵÄĪļÖŹµÄĮæÅضČĪŖ0.1mol/L | B£® | Ģ¼ĖįÄʵÄĪļÖŹµÄĮæĪŖ0.1mol | ||
| C£® | c£ØNa+£©=0.2mol/L | D£® | c£ØNa+£©=2mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | H2SO4 | B£® | NH3•H2O | C£® | NaOH | D£® | ŅŅ“¼ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com