
| A. | 均不能与酸反应 | B. | 均能与水直接化合生成酸 | ||
| C. | 能与碱反应生成盐和水 | D. | 不可能是金属氧化物 |
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(葡萄糖aq)+6O2$\stackrel{酶}{→}$6CO2+6H2O | |
| B. | CH3COOH+KOH?CH3COOK+H2O | |
| C. | A+B?C+D;△H<0 | |
| D. | 反应物所具有的总能量小于生成物所具有的总能量的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中金属元素与非金属元素交界线附近的元素既具有一定的金属性也具有一定的非金属性,所以它们属于过渡元素 | |
| B. | 若M2+和N2-的核外电子层结构相同,则原子序数:N>M | |
| C. | 元素周期表的短周期元素中,最外层电子数是其电子层数2倍的元素共有4种 | |
| D. | 在元素周期表中,原子序数差值为2的两种元素有可能处于同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
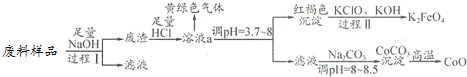
| 温度范围(℃) | 固体质量(g) |
| 150-210 | 4.41 |
| 290-320 | 2.41 |
| 890-920 | 2.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 | |
| C. | 所有的共价化合物都是弱电解质,所有的离子化合物都是强电解质 | |
| D. | 强酸、强碱及大部分盐类都属于强电解质,弱酸、弱碱都属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L氧气含氧分子数约为3.01×1023个 | |
| B. | 两个体积相同的容器,一个盛有NO,另一个盛有N2和O2的混合气体,在同温同压下两容器内气体分子总数、原子总数和气体质量也一定相等 | |
| C. | 标况下,等质量的O2和O3中所含的氧原子数目相等 | |
| D. | 将98gH2SO4溶于500ml水,得到溶液的物质的量浓度为2.0mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com