
下列叙述正确的是( )
|
| A. | 锥形瓶可用作加热的反应器 |
|
| B. | 室温下,不能将浓硫酸盛放在铁桶中 |
|
| C. | 配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高 |
|
| D. | 用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
| 间接加热的仪器及使用方法;化学试剂的存放;试纸的使用;溶液的配制.. | |
| 专题: | 实验评价题. |
| 分析: | A.锥形瓶可用于加热,加热时需要垫上石棉网; B.浓硫酸在室温下能够与铁发生钝化,阻止了铁与浓硫酸的反应; C.俯视刻度线,会导致加入的蒸馏水体积偏小; D.需要根据溶液的酸碱性进行判断,如果溶液为酸性溶液,稀释后溶液的pH偏高,如果为中性溶液,溶液的pH不变. |
| 解答: | 解:A.锥形瓶在制取气体的简易装置中经常作反应容器,不过加热时需要垫上石棉网,故A正确; B.室温下,由于铁与浓硫酸发生钝化,所以能将浓硫酸盛放在铁桶中,故B错误; C.定容时俯视,液面在刻度线下方,溶液的体积偏小,所配溶液浓度偏高,故C正确; D.用蒸馏水润湿的试纸测溶液的pH,若待测液为碱性溶液,则测定结果偏低;若待测液为中性溶液,测定结果不变,若待测液为酸性溶液,测定结果会偏高,所以测定结果不一定偏低,故D错误; 故选AC. |
| 点评: | 本题考查了常见仪器的使用方法、一定物质的量浓度的溶液配制方法、铁与浓硫酸的钝化、试纸的使用方法判断等知识,题目难度中等,注意掌握常见仪器的构造及正确使用方法、配制一定物质的量浓度的溶液方法,明确pH试纸是使用方法. |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
4种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
| M | N | ||
| X | Y |
(1)元素X在周期表中的位置是第________周期、第________族,其单质可采用电解熔融________的方法制备。
(2)M、N、Y三种元素最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是________。(填化学式)
(3)气体分子(MN)2的电子式为________。(MN)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g)+236.6kJ
CH3-C≡C-CH3(g)+2H2(g)→CH3CH2CH2CH3(g)+272.7kJ
 由此不能判断
由此不能判断
A.1,3-丁二烯和2-丁炔稳定性的相对大小
B.1,3-丁二烯和2-丁炔分子储存能量的相对高低
C.1,3-丁二烯和2-丁炔相互转化的热效应
D.一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)===3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
①上述反应中,副产物矿渣可用来________。
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)===6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
2Ca3(PO4)2(s)+10C(s)===P4(g)+6CaO(s)+10CO(g) ΔH2
SiO2(s)+CaO(s)===CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=____________。
(2)(江苏)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)===Cu2+(aq)+H2(g)
ΔH1=+64.39 kJ·mol-1
②2H2O2(l)===2H2O(l)+O2(g)
ΔH2=-196.46 kJ·mol-1
③H2(g)+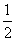 O2(g)===H2O(l)
O2(g)===H2O(l)
ΔH3=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在工业生产和日常生活中有着重要的应用.下列说法正确的是( )
|
| A. | 陶瓷、水泥和光导纤维均属于硅酸盐材料 |
|
| B. | Na2O2、H2O2所含化学键完全相同,都能作供氧剂 |
|
| C. | 常温下,浓硫酸、浓硝酸与铝均能发生钝化,均能用铝罐储运 |
|
| D. | NaClO和明矾都能作消毒剂或净水剂,加入酚酞试液均显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述正确的是( )
|
| A. | 除去水中的Na+、SO42﹣、Cl﹣等杂质可用蒸馏的方法 |
|
| B. | 除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
|
| C. | 用铂丝蘸取少量某溶液进行焰色反应,若火焰呈黄色,则原溶液含有钠盐 |
|
| D. | 某溶液加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液含有SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到相应目的是( )
|
| A. |
制备少量的氧气 |
|
| B. |
证明氧化性Cl2>Br2>I2 |
|
| C. |
将海带灼烧成灰 |
|
| D. |
说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的值,下列叙述正确的是
A.1.00 mol·L-1 NaCl溶液中含有Na+的数目为NA
B.常温常压下,6.4 g由氧气和臭氧组成的混合物中含有的分子总数为0.2NA
C.标准状况下,1.12 L HCHO中C原子的数目为0.05 NA
D.一定条件下6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com