
对已达化学平衡的下列反应:2X(g)+Y(g) 2Z(g)减小压强时,对反应产生的影响是 ( )
2Z(g)减小压强时,对反应产生的影响是 ( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
某无色溶液中只可能含有Na+、Ba2+、Cl-、Br-、SO 、SO
、SO ,对该溶液进行下列实验,实验操作和现象如下表:
,对该溶液进行下列实验,实验操作和现象如下表:
| 步骤 | 操作 | 现象 |
| (1) | 取少量溶液滴加几滴石蕊试液 | 溶液变蓝 |
| (2) | 另取少量溶液滴加过量氯水,再加入CCl4溶液,振荡,静置 | 上层无色,下层呈橙红色 |
| (3) | 取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 | 有白色沉淀产生 |
| (4) | 向(3)的滤液中加入过量AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是( )
A.可能含有Cl-、SO 、SO
、SO B.肯定没有Ba2+、Cl-、Br-
B.肯定没有Ba2+、Cl-、Br-
C.不能确定Na+、SO 、SO
、SO D.肯定含有Na+、Br-、SO
D.肯定含有Na+、Br-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
常见非金属元素及化合物的特征性质和应用
(1)C、N、O、Si、S、Cl等元素形成的单质中:
①属于空气主要成分的是__________,它们相互反应的化学方程式
________________________________________________________________________;
②常用于自来水消毒的是________,它与NaOH溶液反应的离子方程式
________________________________,实验室制备该气体的化学方程式
________________________________________________________________________;
③属于半导体材料的是__________,其工业制取方法是
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某化学研究小组为探究在酒精喷灯加热条件下FeSO4分解的气体产物,进行了一系列实验。已知SO3的熔点是16.8 ℃,沸点是44.8 ℃。
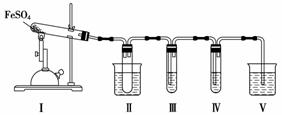
请回答下列问题:
(1)装置Ⅱ的试管中不装任何试剂,其作用是__________________________,试管浸泡在50 ℃的水中,其目的是____________________。
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验中气体产物的成分。请完成实验设计,填写检验试剂、预期现象与结论。限选试剂:3 mol·L-1 H2SO4溶液、6 mol·L-1 NaOH溶液、0.5 mol·L-1 BaCl2溶液、0.5 mol·L-1 Ba(NO3)2溶液、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水。
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中装有______________ | 产生大量白色沉淀,证明气体产物中含有SO3 |
| 装置Ⅳ的试管中装有____________ |
(3)装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是__________。
(4)已知在过量的FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
①甲同学推测该反应的还原产物有两种可能:a.Cl2、b:Cl-。
乙同学结合甲同学的推测,认为其中一种可能可以排除,你认为可以排除的是哪种可能,并用简要的文字和离子方程式说明理由:________________。
②上述反应的离子方程式为__________________。
③为检验上述反应中的还原产物,请选择所需实验步骤,并按先后次序排列:__________(填序号)。
A.取一支试管,加入上述反应后的溶液少许
B.加入过量Ba(NO3)2溶液,出现白色沉淀
C.过滤;取滤液加入硝酸酸化的AgNO3溶液,出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 2SO3(g);△H=-QkJ/mol(Q>0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g);△H=-QkJ/mol(Q>0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
I II III
A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
B.图II研究的是t0时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较低
查看答案和解析>>
科目:高中化学 来源: 题型:
将2 mol X和2 mol Y充入2 L密闭容器中发生如下反应:X(g)+3Y(g)⇌2Z(g)+aQ(g)。2 min达到平衡时生成0.8 mol Z,测得Q的浓度为0.4 mol/L,下列叙述错误的是( )
A.a的值为1 B.平衡时X的浓度为0.8 mol/L
C.Y的转化率为60% D.反应速率v(Y)=0.3 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行反应:H2(g)+Br2(g) 2HBr(g) ΔH<0,达到平衡后,欲使颜色加深,应采取的措施是( )。 A.升高温度 B.降低温度 C.增大H2浓度 D.减小压强
2HBr(g) ΔH<0,达到平衡后,欲使颜色加深,应采取的措施是( )。 A.升高温度 B.降低温度 C.增大H2浓度 D.减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
将pH=3的盐酸a L分别与下列三种溶液混合后,混合液均呈中性
①b L 1×10-3mol·L-1的氨水 ②c L cOH-)=1×10-3mol·L-1的氨水 ③d L cOH-)=1×10-3mol·L-1的BaOH)2溶液,其中a、b、c、d的关系正确的是
)。
A.b>a=d>c B.a=b>c>d
C.a=b>d>c D.c>a=d>b
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定环境中一定能大量共存的是( )
A.无色溶液中:K+、Fe2+、SO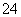 、CO
、CO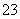
B.存在较多Fe3+的溶液中:Na+、Cl-、SO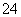 、H+
、H+
C.常温下由水电离出的c(H+)水·c(OH-)水=10-24的溶液中:NH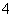 、Cl-、CO
、Cl-、CO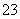 、F-
、F-
D.能使pH试纸变红的溶液中:K+、S2-、CO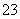 、NO
、NO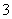
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com