
����Ŀ��Fe@Fe2O3��������һ�������������ϣ��ڴ�������ҽҩ��������ѧ��������й���Ӧ��ǰ����ij�о�С���Գ��ࣨ��������ȡ�����������в����Ĺ���������SiO2��Fe2O3��Al2O3��Ϊԭ�ϣ�������������Ʊ�Fe@Fe2O3�����߲�̽������ˮ�����е�Ӧ�á�
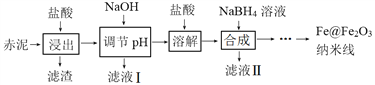
�ش��������⣺
��1����������ʵ���У�������ʼŨ�ȶ������������ʵ�Ӱ����ͼ��ʾ��
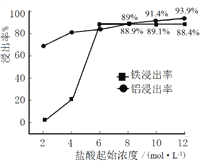
������ĺ���Ũ��Ϊ______________��
��������ʼŨ��Ϊ2 mol��L��1ʱ�����Ľ����ʺܵͣ�ԭ����______________��
��2����֪��25��ʱ��Al(OH)3(s)![]() AlO2��+ H+ + H2O K=4��10��13��������Һc(Al3+) = 0.04 mol��L��1��������pH��ʱ��pH��СӦΪ______________�������pH��������Һ������䣩��
AlO2��+ H+ + H2O K=4��10��13��������Һc(Al3+) = 0.04 mol��L��1��������pH��ʱ��pH��СӦΪ______________�������pH��������Һ������䣩��
��3��Fe@Fe2O3������Ϊ�Dz�ṹ������Fe������Fe2O3�������������������ںϳɹ����б��������γɡ�
�١��ϳɡ�ʱ�μ�NaBH4��Һ�����а������ݲ�������Һ���к�B(OH)3���ϳ����˵����ӷ���ʽΪ____________________________��
�ڡ��ϳɡ������ˡ�______________��______________���Fe@Fe2O3�����ߡ�
��4��Fe@Fe2O3������ȥ��ˮ����Cr2O72���Ļ����ǣ������߽�Cr2O72�������ڱ��沢��ԭ���ڡ��������͡������������½������߷ֱ�����������ͬ��ˮ���У�80 min����ո������ߣ���������Ԫ�ص�ԭ�Ӹ��������±���

����ˮ����Fe@Fe2O3�������γɵķ�ɢϵ��____________________________��
������2��ʵ��������______________���������������������
����֪ˮ���м�ⲻ��Cr(��)������1��Fe@Fe2O3�����ߵı���Cr(��)��ȥ����Ϊ____________________________��
���𰸡� 6 mol��L��1 ������ʼŨ��Ϊ2mol��L��1ʱ��Fe3+������ˮ�� 11 9H2O + 4Fe3+ + 3BH4�� = 4Fe + 6H2��+ 3B(OH)3 + 9H+ ϴ�� ��� ���� ���� 46.8%
����������1������ͼ����Ϣ��֪�������Ũ��Ϊ6 mol��L��1ʱ�������Ľ������Ѿ��ܸߣ�������Ũ�Ƚ������������ԣ��ʺ���Ũ��Ϊ6 mol��L��1����������ʼŨ��Ϊ2mol��L��1ʱ��Fe3+������ˮ�⣬���Ľ����ʺܵͣ���2����֪��25��ʱ��Al(OH)3(s)![]() AlO2��+ H+ + H2O K=c(AlO2��)c(H+)= c(Al3+)c3(OH-)=4��10��13��������Һc(Al3+) = 0.04 mol��L��1����Ksp[Al(OH)3]=c(Al3+)c3(OH-)= 0.4 mol��L��1��c3(OH-)=4��10��13��c(OH-)=10��3��������pH��ʱ��pH��СӦΪ11����3���١��ϳɡ�ʱ�μ�NaBH4��Һ�����а������ݲ���Ϊ��������Һ���к�B(OH)3���ϳ����˵����ӷ���ʽΪ9H2O + 4Fe3+ + 3BH4�� = 4Fe + 6H2��+ 3B(OH)3 + 9H+��
AlO2��+ H+ + H2O K=c(AlO2��)c(H+)= c(Al3+)c3(OH-)=4��10��13��������Һc(Al3+) = 0.04 mol��L��1����Ksp[Al(OH)3]=c(Al3+)c3(OH-)= 0.4 mol��L��1��c3(OH-)=4��10��13��c(OH-)=10��3��������pH��ʱ��pH��СӦΪ11����3���١��ϳɡ�ʱ�μ�NaBH4��Һ�����а������ݲ���Ϊ��������Һ���к�B(OH)3���ϳ����˵����ӷ���ʽΪ9H2O + 4Fe3+ + 3BH4�� = 4Fe + 6H2��+ 3B(OH)3 + 9H+��
�ڡ��ϳɡ������ˡ�ϴ�ӡ���ɻ��Fe@Fe2O3�����ߣ���4������ˮ����Fe@Fe2O3�������γɵķ�ɢϵ�ǽ��������ɱ������ݿ�֪��Fe:O:Cr=5.2:16.7:1����CrΪ1mol�������Cr2O72����֪����3.5mol��ʣ�����Ϊ16.7-3.5=13.2mol������Ϊ�������е���������![]() ���������Ϊ5.2mol���ʲ����ϣ���Ӧ���в����������������еģ�������2��ʵ������������������֪ˮ���м�ⲻ��Cr(��)�����������и�Ԫ�صĺ���������1��Fe@Fe2O3�����ߵı���Cr(��)��ȥ����Ϊ
���������Ϊ5.2mol���ʲ����ϣ���Ӧ���в����������������еģ�������2��ʵ������������������֪ˮ���м�ⲻ��Cr(��)�����������и�Ԫ�صĺ���������1��Fe@Fe2O3�����ߵı���Cr(��)��ȥ����Ϊ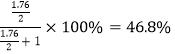 ��
��


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪4NH3��5O2=4NO��6H2O������Ӧ���ʷֱ�����(NH3)����(O2)����(NO)����(H2O)��ʾ������ȷ�Ĺ�ϵ��
A.4��(NH3)��5��(O2)B.5��(O2)��6��(H2O)
C.2��(NH3)��3��(H2O)D.4��(O2)��5��(NO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ�����о�NO2��NO��CO��NO2- �ȴ�����Ⱦ���ˮ��Ⱦ��Ĵ����Խ��������й�������Ҫ���塣
��1����֪����NO2 + CO ![]() CO2 + NO �÷�Ӧ��ƽ�ⳣ��ΪK1����ͬ��
CO2 + NO �÷�Ӧ��ƽ�ⳣ��ΪK1����ͬ��
ÿ1mol�������ʷֽ�Ϊ��̬��̬ԭ�����������ֱ�Ϊ
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
��N2(g)+O2(g) ![]() 2NO(g) ��H��+179.5 kJ/mol K2
2NO(g) ��H��+179.5 kJ/mol K2
��2NO(g) +O2(g)![]() 2NO2(g) ��H��-112.3 kJ/mol K3
2NO2(g) ��H��-112.3 kJ/mol K3
��д��NO��CO��Ӧ��������Ⱦ��������Ȼ�ѧ����ʽ____________________________�Լ����Ȼ�ѧ����ʽ��ƽ�ⳣ��K=____________����K1��K2��K3��ʾ��
��2����Ⱦ������NO2��CO��һ�������µķ�ӦΪ��2NO2+4CO![]() 4CO2+N2��ij�¶��£���1L�ܱ������г���0.1mol NO2��0.2mol CO����ʱ������ѹǿΪ1������ѹ��5��ʱ��Ӧ�ﵽƽ��ʱ��������ѹǿ��Ϊԭ����
4CO2+N2��ij�¶��£���1L�ܱ������г���0.1mol NO2��0.2mol CO����ʱ������ѹǿΪ1������ѹ��5��ʱ��Ӧ�ﵽƽ��ʱ��������ѹǿ��Ϊԭ����![]() ����Ӧ��ʼ��ƽ��ʱCO��ƽ����Ӧ����v(CO)=________��
����Ӧ��ʼ��ƽ��ʱCO��ƽ����Ӧ����v(CO)=________��
�����¶��£�ijʱ�̲��NO2��CO��CO2��N2��Ũ�ȷֱ�Ϊamol/L��0.4mol/L��0.1mol/L��1mol/L��Ҫʹ��Ӧ���淴Ӧ������У�a��ȡֵ��Χ________________��
��3���绯ѧ����NO2-��ԭ������ͼ��
����Դ�ĸ�����____________����A��B��������ӦʽΪ________________��
������������ת����6mol���ӣ���Ĥ������Һ�������仯��![]() Ϊ_____g��
Ϊ_____g��
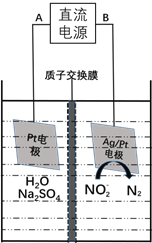
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��ɫ��������Һ���ܹ�������������ǣ�������
A.Al3+��NH4+��NO3����Cl��B.Br����Fe2+��Fe3+��SO42��
C.Na+��SO32����K+��NO3��D.K+��Na+��I ����CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�ij�¶��£���2L������3�����ʼ���з�Ӧ�� X��Y��Z�����ʵ�����ʱ��ı仯������ͼ����Ӧ�� t1min ʱ����ƽ�⣬��ͼ��ʾ��
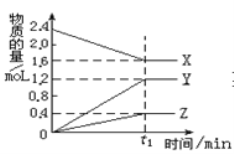
�Ţٸ÷�Ӧ�Ļ�ѧ����ʽ��____________��
�ڸ÷�Ӧ��ƽ�ⳣ����___________��
�� ��t1minʱ���÷�Ӧ�ﵽ��__________״̬�����п���Ϊ�жϷ�Ӧ�Ѵﵽ��״̬����________������ţ���
A��X��Y��Z�ķ�Ӧ������� B��X��Y�����ʵ���Ũ�Ȳ��ٸı�
C������ 3mol Y ��ͬʱ���� 1mol Z D������ 1mol Z ��ͬʱ���� 2mol X
�� ����������Ӧ��X��Y��Z�ֱ�Ϊ NH3 ��H2 ��N2 ������֪1mol�����ֽ�ɵ���������Ҫ����46 kJ������������H2��N2 �ϳ�NH3 ��Ӧ���Ȼ�ѧ��Ӧ����ʽΪ��____________________��
�ڼס�����λͬѧ���۷��ȷ�Ӧ�����ȷ�Ӧ����˵���Ⱥ���ܷ����Ļ�ѧ��Ӧ�����ȷ�Ӧ����˵��Ӧ��Ҫ�������Ȳ��ܽ��еķ�Ӧ�����ȷ�Ӧ������Ϊ����˵����ȷ����__________ͬѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г���Σ�ջ�ѧҩƷ���Ӧ�ķ�����ȷ���ǣ�������
�پƾ������綾Ʒ�� ��Ũ����������ʴƷ�� ������������ȼƷ ��Һ��������������Ʒ���ݸ���������������� �ڻ�ҩ������ըƷ
A.�ڢۢܢ�B.�٢ڢ�C.�٢ܢ�D.�ڢۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ������Ȼ�������о�����ȡ�����½�չ��������ͼװ�ÿɷ�����ӦH2S+O2==H2O2+S����֪�׳��з����ķ�ӦΪ


����˵������ȷ����
A. ��װ���д��ڹ�������ܵ�ת��
B. H+���ҳ�����׳�
C. �ҳ���Һ�з����ķ�ӦΪH2S+I3-===3I-+S+2H+
D. �׳���̿���Ϸ����ĵ缫��ӦΪAQ+2H+-2e-===H2AQ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з��������ڼ����ͪ(CH3COCH3)�ͱ�ȩ����
A. ���ϣȼ�շ� B. ���ڷ� C. ���� D. 1H-NMR��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Zn��һ���������ᷴӦ�����ڷ�Ӧ����̫�죬Ϊ������Ӧ���ʣ����ֲ�Ӱ���������������������������м��������������� �� �� ����
A��NaOH���塡 B��CH3COONa���塡 C��NaCl���� D ��Na2CO3����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com