

分析 在稀硫酸溶液中配置硫酸亚铁氨,加入草酸沉淀沉淀亚铁离子生成草酸亚铁,静置倾去上层溶液后处理得到草酸晶体,
(1)配制(NH4)2Fe(SO4)2•6H2O溶液时,需加少量硫酸的目的是抑制其水解;
(2)沉淀时发生反应硫酸亚铁氨溶液中加入草酸反应生成草酸亚铁沉淀、硫酸和硫酸氨;
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成.说明草酸亚铁被氧化为铁离子、二氧化碳气体,草酸亚铁具有还原性,依据电子守恒计算得到消耗的高锰酸钾物质的量;
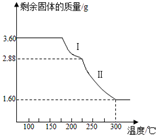
(4)根据图中提供的信息,通过计算可以判断反应的化学方程式和物质的化学式;
①过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶水;
②草酸亚铁晶体中的铁元素质量为:3.6g×$\frac{56}{180}$×100%=1.12g,草酸亚铁晶体中的铁元素完全转化到氧化物中,
氧化物中氧元素的质量为:1.60g-1.12g=0.48g,
铁元素和氧元素的质量比为:1.12g:0.48g=7:3,
据此计算书写化学式.
解答 解:(1)配制(NH4)2Fe(SO4)2•6H2O溶液时,溶液中亚铁离子水解显酸性,需加少量硫酸的目的是抑制其水解,
故答案为:抑制Fe2+水解;
(2)沉淀时发生反应硫酸亚铁氨溶液中加入草酸反应生成草酸亚铁沉淀、硫酸和硫酸氨,反应的化学方程式依据原子守恒配平写出为:(NH4)2Fe(SO4)2+H2C2O4+2H2O=FeC2O4•2H2O↓+H2SO4+(NH4)2SO4,
故答案为:(NH4)2Fe(SO4)2+H2C2O4+2H2O=FeC2O4•2H2O↓+H2SO4+(NH4)2SO4;
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成.说明草酸亚铁被氧化为铁离子、二氧化碳气体,草酸亚铁具有还原性,依据电子守恒计算得到消耗的高锰酸钾物质的量,依据氧化还原反应电子守恒原子守恒配平书写离子方程式为5Fe2++5C2O42-+3MnO4-+24H+=5Fe3++3Mn2++5CO2↑+12H2O,消耗1mol FeC2O4•2H2O,则参加反应的KMnO4为0.6mol;
故答案为:还原性;0.6;
(4)①通过剩余固体的质量可知,过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶水,反应的化学方程式为:FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeC2O4+2H2O
故答案为:FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeC2O4+2H2O;
②草酸亚铁晶体中的铁元素质量为:3.6g×$\frac{56}{180}$×100%=1.12g,草酸亚铁晶体中的铁元素完全转化到氧化物中,
氧化物中氧元素的质量为:1.60g-1.12g=0.48g,
铁元素和氧元素的质量比为:1.12g:0.48g=7:3,
设铁的氧化物的化学式为FexOy,
则有:56x:16y=7:3,
x:y=2:3,
铁的氧化物的化学式为Fe2O3.
故答案为:Fe2O3.
点评 本题考查了铁及其化合物性质的实验验证和实验分析判断,定量计算,图象分析是解题关键,题目难度较大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:
某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 可用溴水区分化合物Ⅱ和化合物Ⅲ | |
| B. | 化合物Ⅰ中所有原子可能在同一平面 | |
| C. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| D. | 1 mol化合物Ⅰ最多能与3 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | COS分子是含有极性键的极性分子 | |
| B. | COS的电子式为: | |
| C. | COS的分子中所有原子满足8电子稳定结构 | |
| D. | COS分子中三个原子处于同一直线上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com