
【题目】下列相关描述正确的是
A.0.1 mol/L 的(NH4) 2SO4 溶液:c(![]() )>c(
)>c(![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
B.0.1 mol/L 的 NaHCO3溶液:c(H+)+c(Na+)=c(OH-)+c(![]() )+2c(
)+2c(![]() )
)
C.常温下恰好中和等体积、相同 pH 的氨水和 NaOH 溶液,消耗盐酸的量相同
D.常温下醋酸钠和醋酸的混合溶液 pH=7,则 c(Na+)>c(CH3COO-)
【答案】B
【解析】
A.(NH4) 2SO4 是强酸弱碱盐,故水解成酸性,即c(H+) >c(OH-),故0.1 mol/L的(NH4) 2SO4 溶液:c(![]() )>c(
)>c(![]() )>c(H+) >c(OH-),A错误;
)>c(H+) >c(OH-),A错误;
B.根据电荷守恒可知,0.1 mol/L的NaHCO3溶液中c(H+)+c(Na+)=c(OH-)+c(![]() )+2c(
)+2c(![]() ),B正确;
),B正确;
C.常温下相同 pH 的氨水和 NaOH 溶液,氨水的浓度远大于NaOH 溶液的浓度,故常温下恰好中和等体积、相同 pH 的氨水和 NaOH 溶液消耗盐酸的量氨水也将远大于NaOH溶液,C错误;
D.常温下醋酸钠和醋酸的混合溶液有电荷守恒式为c(Na+)+ c(H+)=c(CH3COO-)+ c(OH-),当pH=7时,即则c(H+)= c(OH-),故c(Na+)=c(CH3COO-),D错误;
故答案为:B。


科目:高中化学 来源: 题型:
【题目】下列有关物质结构和性质的叙述不正确的是( )
A.甲苯可以被酸性![]() 溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响
溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响
B.苯酚能与氢氧化钠溶液反应而乙醇不能,说明苯环对羟基产生了影响
C.二氯甲烷只有一种结构,说明甲烷的分子构型不是平面型
D.间二甲苯只有一种结构,说明苯环中不存在单双键交替出现的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.1mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述不正确的是
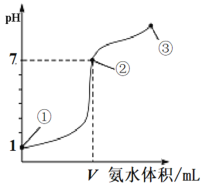
A.V>20 mL
B.①、②、③点水的电离程度大小为:②>③>①
C.在点②所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH![]() )
)
D.在点②、③之间可能存在:c(NH![]() )>c(Cl-)=c(OH-)>c(H+)
)>c(Cl-)=c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、![]() 太阳能电池及铜铟镓硒薄膜太阳能电池等。
太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)基态![]() 原子的价层电子排布式为_______________。
原子的价层电子排布式为_______________。
(2)高温下![]() 容易转化为
容易转化为![]() ,试从原子结构角度解释原因:_______________。
,试从原子结构角度解释原因:_______________。
(3)乙醇的沸点高于乙烷的沸点,其原因是______________。
(4)![]() 的立体构型为________。
的立体构型为________。
(5)硼酸![]() 本身不能电离出
本身不能电离出![]() ,在水中易结合一个
,在水中易结合一个![]() 生成
生成![]() ,而体现弱酸性。
,而体现弱酸性。
①![]() 中含有配位键,其中提供空轨道的是________(填元素符号)。
中含有配位键,其中提供空轨道的是________(填元素符号)。
②![]() 的结构式为________。
的结构式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.向氯化铝溶液中滴加过量氨水:Al3++4NH3·H2O=![]() +4
+4![]() +2H2O
+2H2O
B.浓盐酸与MnO2反应制取Cl2:MnO2+4HCl(浓) ![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
C.酸性条件下,碘化钾溶液露置于空气中变质:4H++4I-+O2=2I2+2H2O
D.向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:![]() +OH-=
+OH-=![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荧光材料硫化锌(ZnS)的研究至今已有 150 多年的历史,可用于制白色颜料、发光粉、发光油漆等,其久置于湿空气中易被氧化为 ZnSO4。请回答下列问题:
(1)基态 Zn 原子的电子排布式为_________________________,核外电子占据最高能层的符号是__________________________, 占据该能层电子的电子云轮廓图形状为__________________________。
(2)ZnSO4 中三种元素的电负性由大到小的顺序为__________________________,![]() 的立体构型为__________________________,其中 S 的杂化轨道类型为__________________________。
的立体构型为__________________________,其中 S 的杂化轨道类型为__________________________。
(3)ZnSO4 溶于氨水可生成[Zn(NH3)4]SO4 溶液,[Zn(NH3)4]SO4 溶液中不存在的微粒间作用力有__________________________。
A.离子键B.共价键C.配位键D.范德华力
(4)根据下列锌卤化物的熔点和溶解性,判断 ZnF2 晶体的类型为______;分析 ZnCl2、ZnBr2、ZnI2 熔点依次增大的原因__________________________。
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
在乙醇、乙醚中的溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
(5) 立方 ZnS 晶体的密度为 ρ g/cm3,其晶胞结构如图。

S2-周围等距离且最近的 Zn2+为__________________________;ZnS晶胞中的晶胞参数 a=__________________________nm(列出计算式)。[ M(ZnS)=97 g/mol ]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中可能大量共存的是
A.澄清透明的溶液中: Fe3+、Mg2+、SCN-、Cl-
B.由水电离产生的c(H+)= 10-13mol/L 的溶液: K+、Na+、CH3COO-、![]()
C.c(Fe2+)= 1mol/L的溶液中: H+、![]() 、
、![]() 、
、![]()
D.pH=1的溶液中: Ba2+、Mg2+、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项比较中前者高于(或大于或强于)后者的是
A. 金属Mg(六方最密堆积)和金属Cu(面心立方最密堆积)的空间利用率
B. BF3和CH4中心原子的价层电子对数
C. Si-O和C-O的键能
D. 对羟基苯甲醛(![]() )和邻羟基苯甲醛(
)和邻羟基苯甲醛(![]() )的沸点
)的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以玉米(主要成分是淀粉)为原料制备乙醇的流程如下:

下列说法中不正确的是
A. C12H22O11属于二糖B. 可采取分液的方法分离乙醇和水
C. 可用碘水检验淀粉是否完全水解D. 葡萄糖可以在酒曲酶作用下分解生成乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com