

分析 (1)碳化钙与水反应生成乙炔,乙炔与溴水发生加成反应;
(2)蒸馏实验需要温度计、蒸馏烧瓶、酒精灯、冷凝管、牛角管、锥形瓶等;
(3)除去苯甲酸晶体中的不溶性杂质,溶解后趁热过滤,减少晶体的损失,再冷却结晶、干燥即可;
(4)分离粗产品乙酸乙酯、乙酸和乙醇的混合物,由流程可知,加试剂a为饱和碳酸钠溶液,操作I为分液,A中含乙酸乙酯,干燥得到A为乙酸乙酯;B中含乙醇、乙酸钠、碳酸钠,操作II为蒸馏,E为乙醇,C中含乙酸钠、碳酸钠,加试剂b为硫酸,D中含硫酸钠、乙酸,Ⅲ为蒸馏,可分离出乙酸,以此来解答.
解答 解:(1)实验室制取乙炔的反应方程式为CaC2+2H2O→Ca(OH)2+C2H2↑,将乙炔净化后通入溴水中,现象为黄色溶液褪色(或变浅),溶液分层,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;黄色溶液褪色(或变浅),溶液分层;
(2)含有杂质的工业乙醇的蒸馏的蒸馏装置中,玻璃仪器有酒精灯、蒸馏烧瓶、温度计、冷凝管、尾接管、锥形瓶,
故答案为:温度计;冷凝管;
(3)除去苯甲酸晶体中的不溶性杂质,实验步骤为:加热溶解,蒸发浓缩,热过滤,冷却结晶,过滤,洗涤,干燥,
故答案为:热过滤;冷却结晶;洗涤;
(4)分离粗产品乙酸乙酯、乙酸和乙醇的混合物,由流程可知,加试剂a为饱和碳酸钠溶液,操作I为分液,A中含乙酸乙酯,干燥得到A为乙酸乙酯;B中含乙醇、乙酸钠、碳酸钠,操作II为蒸馏,E为乙醇,C中含乙酸钠、碳酸钠,加试剂b为硫酸,D中含硫酸钠、乙酸,Ⅲ为蒸馏,可分离出乙酸,
综上所述,试剂a是:饱和Na2CO3溶液,分离方法Ⅰ是分液,分离方法Ⅱ是蒸馏,试剂b是硫酸,
故答案为:饱和Na2CO3溶液;分液;蒸馏;硫酸.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、混合物分离方法、实验流程为解答的关键,侧重分析与实验能力的考查,注意(3)为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
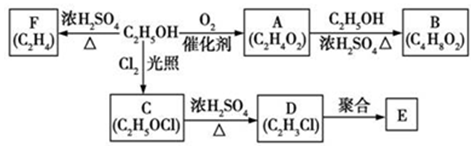
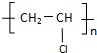 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中一定含有共价键 | |
| B. | 区分离子化合物和共价化合物的方法是看其水溶液是否能导电 | |
| C. | 离子化合物只含离子键 | |
| D. | 离子化合物在熔融状态能够电离出自由移动的离子,而共价化合物不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.08mol/(L•s) | B. | 0.02mol/(L•s) | C. | 0.4mol/(L•s) | D. | 0.2mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能通过加氢反应得到③的烯烃有四种 | |
| B. | ①和②互为同分异构体,①和④互为同系物 | |
| C. | ②可以由烯烃与氢气加成而获得 | |
| D. | ④的一氯代物有四种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3→Fe | B. | Cu→Cu(NO3)2 | C. | SO3→H2SO4 | D. | Al2O3→NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K越大,反应速率越大 | |
| B. | 对任一给定的可逆反应,温度升高,K值增大 | |
| C. | 对可逆反应,K值越大,反应物的转化率越高 | |
| D. | 加入催化剂或增大反应物浓度,K值将增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com