
【题目】下列说法中正确的是( )
A.纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖
B.某有机物结构如图所示 ,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种
,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种
C.含5个碳原子的有机物,每个分子中最多可形成4个C—C单键
D.2,3二甲基丁烷的H—NMR上有5个峰
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3并达到平衡。若在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则关于甲、乙两容器说法正确的是( )
2SO3并达到平衡。若在这一过程中,甲容器保持体积不变,乙容器保持压强不变,则关于甲、乙两容器说法正确的是( )
A. 达平衡时间甲比乙短
B. 乙容器中再充入等物质的量的SO2和O2,重新达平衡时转化率减小
C. 达平衡时,甲中SO2的浓度比乙中SO2的浓度大
D. 达平衡时,甲的转化率比乙低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸的黄铁矿烧渣(主要成分为Fe2O3及少量的FeS、SiO2、Cu、Au、Ag等)是工业三废之一,其综合利用是一条变废为宝的重要途径。
I.以黄铁矿烧渣为原料制备颜料铁红(Fe2O3)和回收(NH4)2SO4的生产工艺流程如下图:
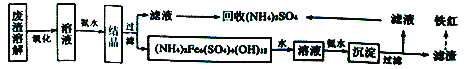
请回答下列问题:
(1)能提高“废渣溶解”速率的措施有______(写出一条即可),“氧化”的目的是______________。 (2)(NH4)2Fe6(SO4)4(OH)12中Fe的化合价是__________________。
(3)该工艺流程图中,第二次加入氨水后,反应的离子方程式为________________________。
II.下图是以黄铁矿烧渣为原料制备颜料铁红的另外一种生产工艺流程:
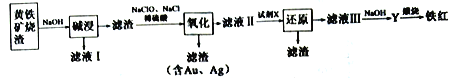
(4)在滤液I中加入廉价的熟石灰,反应的化学方程式是___________________。
(5)“氧化”反应较多,其中FeS 可以看做被水溶液中Cl2氧化,氧化后的溶液中滴加BaCl2有不溶解于盐酸的白色沉淀生成,则水溶液中FeS 与Cl2 反应的离子方程式为________________。
(6)试剂X 为过量铁粉,其作用是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是胶体 ②是溶液 ③能产生丁达尔效应 ④不能透过滤纸 ⑤能透过滤纸 ⑥能透过半透膜
A. ①③⑤ B. ②③④ C. ②③⑤ D. ①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三种有机物是某些药物中的有效成分

下列说法正确的是( )
A. 三种有机物都能发生水解反应
B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C. 将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸消耗氢氧化钠最多
D. 使用FeCl3溶液和稀硫酸可以鉴别这三种有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铁及其化合物的说法不正确的是( )
A.Fe2O3俗称铁红
B.用FeCl3溶液作刻制印刷电路的“腐蚀液”
C.常温下可用铁制容器盛装浓硫酸或浓硝酸
D.水蒸气通过灼热的铁粉生成氢氧化铁和氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。回答下列问题:
(1)0.3mol NH3分子中所含原子数与__________个H2O分子中所含原子数相等。
(2)含0.4mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是__________
(3)—定条件下,16g A和20g B恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为__________
(4)某混合盐溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为: 0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO42-) =__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用废弃固体(含有Cu2S、Al2O3、Fe2O3、SiO2等)制取粗铜、绿矾(FeSO4·7H2O)和明矾[KAl(SO4)2·12H2O],操作流程如下:

(1)气体a是_________(写化学式,下同),试剂X是_________(已知X是一种盐),固体C是_________。
(2)明矾可以净水,明矾净水的原理是____________________________________(用离子方程式表示)。
(3)利用反应2Cu+O2+2H2SO4![]() 2CuSO4+2H2O可制备CuSO4,若将该反应设计成原电池,该电池的正极反应式为_______________________。
2CuSO4+2H2O可制备CuSO4,若将该反应设计成原电池,该电池的正极反应式为_______________________。
(4)取少量产品绿矾,加水溶解后再滴入几滴KSCN溶液,若产品绿矾中不含有Fe3+,观察到的现象为_________;若在产品绿矾的水溶液中滴加酸性高锰酸钾溶液,观察到的现象为__________________,原因是____________________________ (用离子方程式表示)。
(5)已知绿矾受热分解的化学方程式为2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O。称取3.5g产品绿矾,加热分解至恒重后(杂质受热不分解),将反应所得的气体缓缓通入盛有足量蒸馏水的锥形瓶中,再用0.1000 mol·L-1的酸性KMnO4溶液滴定,滴定到终点时消耗酸性KMnO4溶液的体积为25.00mL,则产品绿矾的纯度为__________ (保留三位有效数字)。
Fe2O3+SO2↑+SO3↑+14H2O。称取3.5g产品绿矾,加热分解至恒重后(杂质受热不分解),将反应所得的气体缓缓通入盛有足量蒸馏水的锥形瓶中,再用0.1000 mol·L-1的酸性KMnO4溶液滴定,滴定到终点时消耗酸性KMnO4溶液的体积为25.00mL,则产品绿矾的纯度为__________ (保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)MgCl2固体中含离子总数为1.806×1024个,将其配成2000mL溶液,求:
①c(MgCl2)=_____。
②c(Cl-)=____。
(2)配制500mL含Fe3+56g的Fe2(SO4)3溶液,需要6.25mol/L的Fe2(SO4)3溶液的体积为___mL。
(3)______mL 2 mol/L的NaOH溶液中所含溶质的质量和200mL 1 mol/L的Na2SO4溶液所含溶质的质量相等。
(4)11.7克NaCl配制成100mL溶液,此溶液中c(Cl-)与标准状况下44.8升HCl配成V L溶液中的c(Cl-)相等,求V=______。
(5)含34.2g Al2(SO4)3的溶液,其体积与0.5mol/L含Na2SO4质量为142g的溶液体积相同。求该Al2(SO4)3溶液中c(SO42-)=__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com