
·ÖĪö £Ø1£©øł¾Ż·“Ó¦¢ŁµÄĘ½ŗā³£ŹżK±ķ“ļŹ½ĪŖ£ŗK=$\frac{c£ØPC{l}_{3}£©c£ØC{l}_{2}£©}{c£ØPC{l}_{5}£©}$=1£¬Ōņc£ØPCl3£©•c£ØCl2£©=c£ØPCl5£©£»Ę½ŗā³£ŹżĪŖÉś³ÉĪļµÄÅضČĆŻÖ®»żÓė·“Ó¦ĪļÅضČĆŻÖ®»żµÄ±ČÖµ£»
£Ø2£©Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹżĆŻÖ®»ż³żŅŌ·“Ó¦ĪļµÄÅØ¶ČµÄ»Æѧ¼ĘĮæŹżĆŻÖ®»ż£¬ÓÉÓŚ·“Ó¦¢Ū=¢Ł+¢Ś£¬¹ŹK3=K1”ĮK2£¬¾Ż“Ė¼ĘĖć£»
£Ø3£©KŹĒĪĀ¶ČµÄŗÆŹż£¬ĪĀ¶Č²»±äK²»±ä£»
£Ø4£©øł¾Ż·“Ó¦µÄĪüČČ»ņ·ÅČČĢŲµć£¬øıäĪĀ¶ČŹ¹Ę½ŗāĻņijŅ»·½ĻņŅĘ¶Æ£¬æÉøıäĘ½ŗā³£ŹżµÄ“󊔣®
½ā“š ½ā£ŗ£Ø1£©øł¾Ż·“Ó¦¢ŁæÉÖŖĘ½ŗā³£ŹżK±ķ“ļŹ½ĪŖ£ŗK=$\frac{c£ØPC{l}_{3}£©c£ØC{l}_{2}£©}{c£ØPC{l}_{5}£©}$=1£¬Ōņc£ØPCl3£©•c£ØCl2£©=c£ØPCl5£©Ņ»¶Ø³ÉĮ¢£»
¹Ź“š°øĪŖ£ŗC£»
£Ø2£©Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹżĆŻÖ®»ż³żŅŌ·“Ó¦ĪļµÄÅØ¶ČµÄ»Æѧ¼ĘĮæŹżĆŻÖ®»ż£¬¢ŚCO£Øg£©+Cl2£Øg£©?COCl2£Øg£©£»”÷H1£¼0 K2=5”Į104L•mol-1£¬¢ŪCOCl2£Øg£©?CO£Øg£©+Cl2£Øg£©Äę·“Ó¦£¬Ę½ŗā³£ŹżK3=$\frac{1}{{K}_{2}}$=$\frac{1}{5”Į1{0}^{4}}$=2”Į10-5 mol•L-1£¬
¹Ź“š°øĪŖ£ŗ2”Į10-5 mol•L-1£»
£Ø3£©KŹĒĪĀ¶ČµÄŗÆŹż£¬ĪĀ¶Č²»±äK²»±ä£¬ĖłŅŌ½µµĶCl2ÅØ¶Č£¬K²»±ä£¬¹Ź“š°øĪŖ£ŗ²»±ä£»
£Ø4£©ŅŖŹ¹·“Ó¦¢ŁŗĶ·“Ó¦¢ŚµÄKÖµĻąµČ£¬
A”¢·“Ó¦¢Ł”¢·“Ó¦¢ŚĶ¬Ź±ÉżøßĪĀ¶Č£¬Ōņ¢Ł·“Ó¦Ę½ŗāÓŅŅĘ£¬¢Ś·“Ó¦Ę½ŗā×óŅĘ£¬KæÉÄÜĻąµČ£¬¹ŹÕżČ·£»
B”¢·“Ó¦¢Ł”¢·“Ó¦¢ŚĶ¬Ź±½µµĶĪĀ¶Č£¬Ōņ¢Ł·“Ó¦Ę½ŗā×óŅĘ£¬K¼õŠ”£¬¢Ś·“Ó¦Ę½ŗāÓŅŅĘ£¬KŌö“󣬶žÕß²»æÉÄÜĻąµČ£¬¹Ź“ķĪó£»
C”¢·“Ó¦¢Ł½µµĶĪĀ¶Č£¬Ōņ¢Ł·“Ó¦Ę½ŗā×óŅĘ£¬K¼õŠ”£¬·“Ó¦¢ŚĪ¬³Ö210”ę£¬¶žÕß²»æÉÄÜĻąµČ£¬¹Ź“ķĪó£®
¹Ź“š°øĪŖ£ŗA£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā³£ŹżµÄŗ¬Ņ壬×öĢāŹ±×¢Ņā°ŃĪÕĘ½ŗā³£ŹżµÄÓ°ĻģŅņĖŲÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬“ĖĪŖ»ÆŃ§Ę½ŗā³£æ¼²éĪŹĢā£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 »Ŗ¶«Ź¦“ó°ęŅ»æĪŅ»Į·ĻµĮŠ“š°ø
»Ŗ¶«Ź¦“ó°ęŅ»æĪŅ»Į·ĻµĮŠ“š°ø ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ŅŅ“¼ | 1£¬2-¶žäåŅŅĶé | ŅŅĆŃ | |
| דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
| ĆܶČ/g•cm-3 | 0.79 | 2.2 | 0.71 |
| ·Šµć/”ę | 78.5 | 132 | 34.6 |
| ČŪµć/”ę | Ņ»l30 | 9 | -1l6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2O | B£® | H2SO4 | C£® | NaH | D£® | NH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O | B£® | Fe2O3ŗĶFe | C£® | Fe2O3 | D£® | Fe2O3ŗĶNaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ļµ½»ÆŃ§Ę½ŗāŹ±£¬4¦ŌÕż£ØO2£©=5¦ŌÄę£ØNO£© | |
| B£® | Čōµ„Ī»Ź±¼äÄŚÉś³ÉxmolNOµÄĶ¬Ź±£¬ĻūŗÄxmolNH3£¬Ōņ·“Ó¦“ļµ½Ę½ŗāדĢ¬ | |
| C£® | “ļµ½»ÆŃ§Ę½ŗāŹ±£¬ČōŌö¼ÓČŻĘ÷Ģå»ż£¬ŌņÕż·“Ó¦ĖŁĀŹ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹŌö“ó | |
| D£® | »Æѧ·“Ó¦ĖŁĀŹ¹ŲĻµŹĒ£ŗ2¦ŌÕż£ØNH3£©=3¦ŌÕż£ØH2O£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.6gĢś·ŪŌŚ0.1molĀČĘųÖŠ³ä·ÖČ¼ÉÕ£¬×ŖŅʵē×ÓŹżĪŖ0.3NA | |
| B£® | 2.5mL 16mol•L-1ÅØĮņĖįÓė×ćĮæĶ·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.04NA | |
| C£® | 7.8g Na2SŗĶNa2O2µÄ¹ĢĢå»ģŗĻĪļÖŠŗ¬ÓŠµÄŅõĄė×ÓŹżµČÓŚ0.1NA | |
| D£® | ³£ĪĀĻĀ£¬5.6gĢś¶¤Óė×ćĮæÅØĻõĖį·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¹¤ŅµÉś²śĻõĖįµÄĪ²ĘųÖŠŗ¬ÓŠµŖŃõ»ÆĪļNOx£ØNOŗĶNO2µÄ»ģŗĻĪļ£¬¼ŁÉč²»ŗ¬N2O4£©£¬¶ŌÉśĢ¬»·¾³ŗĶČĖĄą½”浓ųĄ“½Ļ“óµÄĶžŠ²£®
¹¤ŅµÉś²śĻõĖįµÄĪ²ĘųÖŠŗ¬ÓŠµŖŃõ»ÆĪļNOx£ØNOŗĶNO2µÄ»ģŗĻĪļ£¬¼ŁÉč²»ŗ¬N2O4£©£¬¶ŌÉśĢ¬»·¾³ŗĶČĖĄą½”浓ųĄ“½Ļ“óµÄĶžŠ²£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 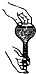 ¼ģ²éČŻĮæĘæŹĒ·ńĀ©Ė® | B£® | 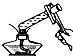 øųČÜŅŗ¼ÓČČ | ||
| C£® | 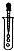 µĪ¼ÓŅŗĢå | D£® | 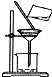 ¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com