
| A. | 工业上从海水中提取金属镁所发生的化学反应中,不涉及的物质是HCl | |
| B. | 工业上用氯气与澄清石灰水反应制取漂白粉 | |
| C. | 工业炼铁中用石灰石除去铁矿石中的脉石 | |
| D. | 工业上通常用氢氧化钠和煤一起混合燃烧,为了避免二氧化硫污染空气 |
分析 A.从海水中提取镁的步骤为:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥产物;④将产物电解得到金属镁;
B.澄清石灰水氢氧化钙浓度低,应该用Cl2与石灰乳制取漂白粉;
C.高炉炼铁时,使用石灰石的目的是:将矿石中的二氧化硅转变为炉渣,即除去脉石(SiO2);
D.为了防止煤燃烧生成二氧化硫污染空气,通常在煤燃烧时加入一些生石灰(CaO),使燃烧时产生的二氧化硫和生石灰(CaO)发生化合反应生成一种固体产物,从而达到固硫的目的.
解答 解:A.把贝壳制成石灰乳,涉及反应:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、CaO+H2O═Ca(OH)2;在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,涉及反应:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;将沉淀物与盐酸反应,结晶、过滤、干燥产物,涉及反应:Mg(OH)2+2HCl=MgCl2+2H2O,MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O;④将产物电解得到金属镁,涉及反应:MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,从海水中提取金属镁所发生的化学反应中,涉及HCl,故A错误;
B.因为澄清石灰水中Ca(OH)2的浓度太小,故应该用Cl2与石灰乳制取漂白粉,故B错误;
C.炼铁时,石灰石中的碳酸钙在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和二氧化硅反应生成硅酸钙,从而除去铁矿石中的二氧化硅,故C正确;
D.高温条件下,二氧化硫和生石灰化合生成了亚硫酸钙,反应的化学方程式是:CaO+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3,从而达到固硫的目的,故D错误;
故选C.
点评 本题考查了有关化学工艺的一些知识,掌握从海水中提取金属镁原理、制取漂白粉的原理、工业炼铁除去铁矿石中的脉石方法、燃煤除硫的原理是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E各物质的转化关系如图所示.
A、B、C、D、E各物质的转化关系如图所示. ;
;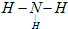 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl是还原产物,KClO3是氧化产物 | |
| B. | KOH在该反应中体现碱性和还原性 | |
| C. | 反应中每消耗3 mol Cl2,转移电子数为5NA | |
| D. | 被还原的氯气的物质的量是被氧化的氯气的物质的量的5倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠投入到CuSO4溶液中:2Na+Cu2+═Cu↓+2Na+ | |
| B. | 澄清石灰水中加过量小苏打:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 氢氧化铝中滴入足量盐酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | 四氧化三铁粉末投入到足量盐酸中:Fe3O4+8H+═3Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$
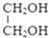 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$ +H2O
+H2O =
= =
=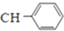
 ;由G、E生成N的反应类型是取代反应.
;由G、E生成N的反应类型是取代反应. D的结构简式:
D的结构简式: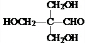

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体通入Na2SiO3溶液中 | B. | SO2气体通入Ca(OH)2溶液中 | ||
| C. | CO2气体通入饱和Na2CO3溶液中 | D. | SO2气体通入CaCl2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 陶瓷的主要成分是硅酸盐 | B. | 硅可用作半导体材料 | ||
| C. | 电解氯化钠溶液制取金属钠和氯气 | D. | 铁槽可存放冷的浓硝酸、浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com