
【题目】某研究小组将一批电子废弃物简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计如下制备硫酸铜晶体和无水氯化铁的方案:

已知:Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O
请回答下列问题:
(1)步骤①Cu与酸反应的离子方程式为_________________________。
(2)步骤②加H2O2的作用是______________,滤渣2为(填化学式)__________。
(3)步骤⑤不能直接加热脱水的理由是________
(4)若滤液1中Cu2+的浓度为0.02mol·L-1,则氢氧化铜开始沉淀时的pH=________(已知:Ksp[Cu(OH)2]=2.0x10-20)
(5)已知:2Cu2++4I-=2CuI↓+I2 I2+2S2O32-=2I-+S4O62-
某同学为了测定CuSO4·5H2O产品的质量分数可按如下方法:取3.00g产品,用水溶解后,加入足量的KI溶液,充分反应后过滤、洗涤,将滤液稀释至250mL,取50mL加入淀粉溶液作指示剂,用0.080mol·L-1Na2S2O3标准溶液滴定,达到滴定终点的依据是______________。
四次平行实验耗去Na2S2O3标准溶液数据如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
此产品中CuSO4·5H2O的质量分数为__________。
【答案】 Cu+4H++2NO3-= Cu2+ +2NO2↑+2H2O, 3Cu+8H++2NO3-![]() 3Cu2+ +2NO↑+4H2O 将 Fe2+氧化成 Fe3+ Fe(OH)3、A1(OH)3 FcCl3易水解:FeCl3+3H2O
3Cu2+ +2NO↑+4H2O 将 Fe2+氧化成 Fe3+ Fe(OH)3、A1(OH)3 FcCl3易水解:FeCl3+3H2O![]() Fe(OH)3+3HCl ,加热能促进FeCl3的水解,蒸干得不到FeCl3 5 溶液由蓝色褪为无色且半分钟内不恢复原色 83. 3%
Fe(OH)3+3HCl ,加热能促进FeCl3的水解,蒸干得不到FeCl3 5 溶液由蓝色褪为无色且半分钟内不恢复原色 83. 3%
【解析】试题分析:(1)浓硝酸与稀硫酸混合后,可能为浓硝酸也可能为稀硝酸,所以离子方程式为:Cu + 4H++ 2NO3 = Cu2++2NO2↑+ 2H2O或3Cu+8H++2NO3![]() 3Cu2++2NO↑+4H2O
3Cu2++2NO↑+4H2O
(2)H2O2具有强氧化性,所以H2O2的作用是将Fe2+氧化成Fe3+;加入足量氨水,Fe3+、Al3+转化为Fe(OH)3沉淀和Al(OH)3沉淀,所以滤渣2为Fe(OH)3、Al(OH)3。
(3)FeCl3为强酸弱碱盐,容易发生水解反应:FeCl3+3H2O![]() Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。
Fe(OH)3+3HCl,加热能促进FeCl3的水解,蒸干得不到FeCl3。
(4)c2(OH)c(Cu2+)= Ksp[Cu(OH)2],代入数据可求出c(OH)=1.0×10-9molL1,pH=-lgc(H+)=-lg【Kw÷c(OH)】=5。
(5)Cu2+把I氧化为I2,加入淀粉溶液变蓝,用Na2S2O3标准溶液滴定,达到滴定终点时,Na2S2O3与I2恰好完全反应,所以达到滴定终点的依据是:溶液由蓝色褪为无色且半分钟内不恢复原色;实验3所测数据明显大于其他3组数据,说明实验3出现了实验错误,应舍去,根据其他3组数据求出平均值,根据2Cu2++4I-= 2CuI↓+I2和I2+2S2O32-= 2I-+S4O62-可得对应关系:S2O32- ~ Cu2+,所以n(CuSO45H2O)=n(Cu2+)=n(S2O32- )=0.080 mol·L-1×(25.00+25.02+24.98)/3L=0.002mol,所以此产品中CuSO4·5H2O的质量分数为:0.002mol×250g/mol×5÷3.00g×100%=83.3%


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为__________________。
利用反应6NO2+8NH3 ![]() 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_________ L。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_________ L。
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=﹣196.6 kJ·mol-1
2SO3(g) ΔH=﹣196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=﹣113.0 kJ·mol-1
2NO2(g) ΔH=﹣113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) 的ΔH=__________kJ·mol-1。
SO3(g)+NO(g) 的ΔH=__________kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于一恒容密闭绝热容器中发生上述反应,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g) ΔH=﹣a kJ·mol-1。
CH3OH(g) ΔH=﹣a kJ·mol-1。
在一定温度下,将1mol CO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则此时v逆(CH3OH)为_____,正反应放出的热量为__________________。
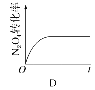
(4)已知N2O4(g) ![]() 2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图不能说明反应达到平衡状态的是________。
2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图不能说明反应达到平衡状态的是________。



查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制若干体积的1.0mol/L Na2CO3溶液,正确的方法是(假设其余各步操作正确无误)( )
A.将10.6g Na2CO3溶于100mL水中
B.将57.2g Na2CO310H2O溶于少量水中,再用水稀释至200mL
C.将20 mL 5.0mol/L Na2CO3溶液用水稀释至100mL
D.将21.2gNa2CO310H2O溶于200mL水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示从原混合物中分离出X的两种方案、下列说法不合理的是

A. 若含X的混合物为溴水,可通过方案I进行分离,加入试剂为CCl4液体,充分振荡后液体分层,下层为X的CC14溶液
B. 若含X的混合物为BaSO4和BaSO3的混合物,可通过方案Ⅱ进行分离,加入试剂为稀硝酸,X为BaSO4
C. 若含X的混合物为乙醇和乙酸乙酯的混合物,可通过方案I进行分离,加入试剂为饱和NaOH溶液,残留液中含有乙酸钠
D. 若含X的混合物为Fe、Al,可通过方案II进行分离,加入的试剂是过量的NaOH溶液,1molX与足量氯气完全反应时,转移3mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 棉花、羊毛、蚕丝均属于天然纤维素
B. 石油的分馏和裂化均属于化学变化
C. 油脂都不能使溴的四氯化碳溶液褪色
D. 甲烷、乙醇、乙酸在一定条件下都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列大小关系正确的是( )
A.熔点:已烷>2—甲基丁烷>戊烷>丁烷
B.分子中氢元素的百分含量:甲烷>乙烷>乙烯>乙炔
C.密度:苯>H2O>CCl4
D.相同物质的量的物质完全燃烧所消耗的氧气的量:已烷>环已烷>苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com