
| A、pH=7的溶液 |
| B、由强酸与强碱等物质的量反应得到的溶液 |
| C、使酚酞试液呈无色的溶液 |
| D、c(H+)=c(OH-)=10-6mol/L的溶液 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | ||
| B、0.1mol/LH2SO4与0.1mol/L氨水等体积混合:c(H+)>c(NH4+)>c(SO42-)>c(OH-) | ||
C、0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:
| ||
| D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NaOH+Cl2═NaCl+NaClO+H2O |
| B、H2+Cl2═2HCl |
| C、2NaCl(熔融)=2Na+Cl2↑ |
| D、2HClO═2HCl+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
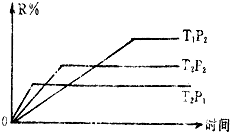 在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )
在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )| A、正反应为吸热反应 L是气体 |
| B、正反应为放热反应 L是气体 |
| C、正反应为吸热反应 L是固体 |
| D、正反应为放热反应 L是固体或液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、氧气压强不变 | ||||
| B、BaO质量增加 | ||||
| C、BaO2质量不变 | ||||
D、平衡常数K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
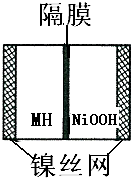 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )| A、放电时正极反应为:NiOOH+H2O+e-═Ni(OH)2+OH- |
| B、电池的电解液可为稀H2SO4溶液 |
| C、充电时负极反应为:MH+OH--e-═H2O+M |
| D、MH是一类储氢材料,其所含氢密度越大,电池的能量密度越高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com